分享:6061铝合金表面ZnAl-LDHs层的制备及其耐腐蚀性能
张玉圣
摘要
采用原位生长的方法,首先在6061铝合金表面制备了层间含NO3-的ZnAl-LDHs (layered double hydroxides,层状双金属氢氧化物)层,然后将正钒酸根(VO43-)和偏钒酸根(VO3-) 2种缓蚀剂离子插入ZnAl-LDHs-NO3层板间,在6061铝合金表面制备了ZnAl-LDHs-VO4和ZnAl-LDHs-VO3层。通过XRD、FT-IR和SEM等技术研究了上述3种ZnAl-LDHs层的晶体结构、成分组成和表面形貌,并分析了ZnAl-LDHs层的生长行为;通过电化学工作站和超景深3D视频显微镜研究了6061铝合金表面3种ZnAl-LDHs层在3.5%NaCl水溶液中的耐腐蚀行为。结果表明,6061铝合金表面原位制备的ZnAl-LDHs层呈片状垂直于基体生长,能够完全覆盖在铝合金表面。与6061铝合金基体相比,含ZnAl-LDHs层的铝合金具有较高的腐蚀电位(Ecorr)、较小的腐蚀电流(Icorr)和较大的电荷转移电阻(Rct)。这说明ZnAl-LDHs层能够明显提高6061铝合金的耐腐蚀性能,可用于6061铝合金表面的防腐蚀保护。在6061铝合金表面的3种ZnAl-LDHs层中,ZnAl-LDHs-VO3的耐腐蚀性能最高。
关键词:
6061铝合金具有较小的密度、较高的强度、良好的成形性以及耐腐蚀性能,广泛应用于航空航天、轨道交通、机械和电力电子等领域[1,2,3,4]。然而,6061铝合金在含有Cl-的介质中,其表面氧化膜易被侵蚀,出现点蚀、晶间腐蚀和应力腐蚀等局部腐蚀,影响铝合金的力学性能,导致构件的使用寿命降低[5,6,7]。通常采用表面涂层工艺来提高铝合金的耐腐蚀性能,其中铬酸盐钝化是最有效的铝合金表面处理工艺,表面形成的钝化膜能明显提高铝合金的耐腐蚀性,对铝合金起到较优的防腐蚀效果[8,9]。但是,由于Cr(VI)及其衍生物的高毒性和致癌性,对环境和人体的危害较大,同时废液处理难度大,欧洲在2007年已禁止在民用领域使用Cr(VI)钝化[10,11]。近十年来,在替代铬酸盐阳极氧化(CAA)方面已有大量研究,如磷酸盐转化膜[12]、硼酸盐转化膜[13]、Ce(III)盐转化膜[14,15]、锆钛盐转化膜[16]等工艺在一定程度上改善了铝合金的耐蚀性。
环境友好型的层状双金属氢氧化物(layered double hydroxides)是一类由带正电荷的层板和层间阴离子堆积而成的无机功能材料[17,18],其可以作为防腐蚀涂层应用于金属材料的防腐蚀。这主要是因为其可在金属材料表面形成一层致密的LDHs膜,能够阻碍溶液中的侵蚀性Cl-与基体材料的接触;同时由于LDHs层间阴离子的可交换性,Cl-可被容纳到层间并与带正电的层板成键,限制了Cl-在层间的移动,延长Cl-到达基体表面的时间[19];另外LDHs可作为缓蚀剂的载体,与溶液中的Cl-接触后,LDHs层间的缓蚀剂会立即释放到金属/电解液界面,阻碍氧化还原反应的进行,进行自我保护[20]。因此将插入缓蚀剂的LDHs应用到铝合金表面,可以实现隔离、捕获、主动释放缓蚀剂的智能防护,提高铝合金的耐腐蚀性能。已有研究[21,22,23]将LDHs应用到镁合金表面,显著提高了镁合金的耐腐蚀性。Buchheit等[24]在2024铝合金表面制备了ZnAl-LDHs层,Zhang等[25]在5005铝合金表面制备了MgAl-LDHs,其表面的LDHs可以提高铝合金的抗腐蚀性能。Tedim等[26,27]采用原位生长的方法在2024铝合金表面制备了含缓蚀剂(V2O74-)的ZnAl-LDHs层,能进一步提高ZnAl-LDHs层的耐腐蚀性能。Iannuzzi等[28,29]研究了不同pH值下钒酸盐的存在形式及其对2024铝合金的缓蚀机理,发现起主要作用的偏钒酸根(VO3-)作为缓蚀剂,其腐蚀抑制效果与铬酸盐相当。然而关于LDHs层插入不同形式钒酸盐的研究较少。
本工作首先在6061铝合金表面原位制备了ZnAl-LDHs-NO3层,然后将VO43-和VO3-作为缓蚀剂插入ZnAl-LDHs层间,制备了ZnAl-LDHs-VO4和ZnAl-LDHs-VO3层。研究了上述3种ZnAl-LDHs层的结构形貌以及生长行为,分析了3种ZnAl-LDHs层在3.5%NaCl (质量分数)水溶液中的耐腐蚀性机理。
实验所用6061铝合金的主要化学成分(质量分数,%)为:Mg 0.80~1.20,Si 0.40~0.80,Cu 0.15~0.40,Zn 0.25,Mn 0.15,Cr 0.04~0.35,Ti 0.15,Fe 0.70,Al余量。采用线切割机将6061铝合金切割为直径14 mm×5 mm的试样;试样用320、500、800和1200号的砂纸逐级打磨,然后用0.1 μm颗粒的金刚石研磨膏抛光,最后用去离子水和无水乙醇超声清洗。将清洗干净的6061铝合金样品先在0.05 mol/L NaOH溶液中浸泡100 s,再在0.05 mol/L HNO3溶液中浸泡300 s,最后用去离子水和无水乙醇超声清洗,吹干待用。
将预处理后的6061铝合金试样浸泡在0.005 mol/L Zn(NO3)2溶液中,在80 ℃水浴中加热4 h,取出试样用去离子水和无水乙醇超声清洗干净保存,获得的样品命名为ZnAl-LDHs-NO3。取ZnAl-LDHs-NO3样品分别浸泡在0.01 mol/L Na3VO4溶液(pH=11)和0.01 mol/L NaVO3溶液(pH=7)中45 ℃水浴加热3 h,最后将样品用去离子水和无水乙醇超声清洗吹干,获得的样品分别命名为ZnAl-LDHs-VO4和ZnAl-LDHs-VO3。
利用X'Pert MPD X射线衍射仪(XRD)表征样品的晶体结构,采用Cu靶Kα线,扫描范围5°~30°,扫描速率为8°/min。利用IRTracer-100 Fourier变换红外光谱仪(FT-IR)确定层间的酸根离子,将LDHs从铝合金表面层刮下与干燥的KBr按照1∶100 (质量比)混合,然后压片测试,扫描范围在4000~400 cm-1。利用带能谱仪(EDS)的Phenom Prox扫描电子显微镜(SEM)观测样品的微观形貌和元素成分组成。利用DVM6超景深3D视频显微镜来观察样品腐蚀后的三维形貌。
电化学腐蚀性能测试使用PARSTAT 4000A电化学工作站,采用三电极体系,参比电极为饱和甘汞电极(SCE),对电极为Pt片电极,工作电极为铝合金样品(采用树脂密封,保留1 cm2的反应面积),腐蚀介质为3.5%NaCl (质量分数)水溶液。极化曲线测试采用动电位分析法,电位扫描速率为5 mV/s,电位扫描范围-0.8~1.0 V。交流阻抗谱(EIS)测试的频率扫描范围为105~10-2 Hz,正弦扰动信号为10 mV,所有样品测试前均待开路电位稳定。
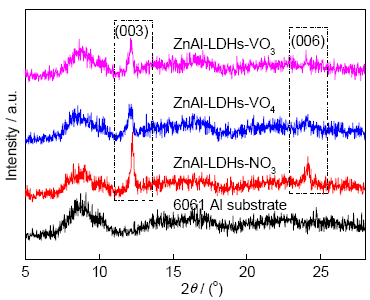
6061铝合金基体及表面不同ZnAl-LDHs层的XRD谱如图1所示。可见,6061铝合金基体在扫描范围(10°~30°)内没有出现明显的衍射峰,3种ZnAl-LDHs层样品在12°和23.5°左右出现2个衍射峰,其分别为ZnAl-LDHs在(003)和(006)的特征衍射峰[30],这说明本工作采用的原位制备方法,在6061铝合金表面成功地制备了ZnAl-LDHs层。ZnAl-LDHs-VO4和ZnAl-LDHs-VO3层的(003)衍射峰比ZnAl-LDHs-NO3向左略微偏移,这是由于VO43-和VO3- 2种阴离子与NO3-经离子交换后插入ZnAl-LDHs层板,引起ZnAl-LDHs层间距的变化,导致其衍射峰发生偏移[31]。
图1 6061铝合金基体及表面不同ZnAl-LDHs层的XRD谱
Fig.1 XRD spectra of 6061 Al substrate and different ZnAl-LDHs films
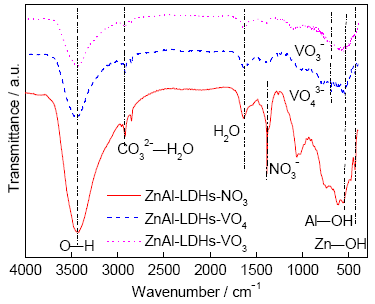
6061铝合金表面原位生成的3种不同ZnAl-LDHs层的FT-IR谱如图2所示。其中3424 cm-1处的峰是由于ZnAl-LDHs层间的酸根离子或层板的金属离子与O—H伸缩振动导致的;2922 cm-1处的峰是由ZnAl-LDHs层间水分子的H键与CO32-键合,产生CO32-—H2O的弹性振动,CO32-是空气中的CO2混入造成的[32];1641 cm-1处的峰是LDHs层间水分子弯曲振动产生的;611 cm-1处的峰是由于Al—OH平移振动产生的;430 cm-1处的峰是由于Zn—OH平移振动产生[33]。3种不同的ZnAl-LDHs层对应的特征峰略有不同,LDHs-NO3样品在1439 cm-1处出现NO3-伸缩振动峰,LDHs-VO4样品在706 cm-1处出现VO43-伸缩振动峰,LDHs-VO3样品在680 cm-1处出现VO3-伸缩振动峰[34],说明通过原位生长法和酸根离子的交换性,在6061铝合金表面制备的LDHs层中插入了不同的酸根离子,这与图1的XRD谱结果一致。
图2 6061铝合金表面不同ZnAl-LDHs层的FT-IR谱
Fig.2 FT-IR spectra of different ZnAl-LDHs films on the 6061 Al alloy surface
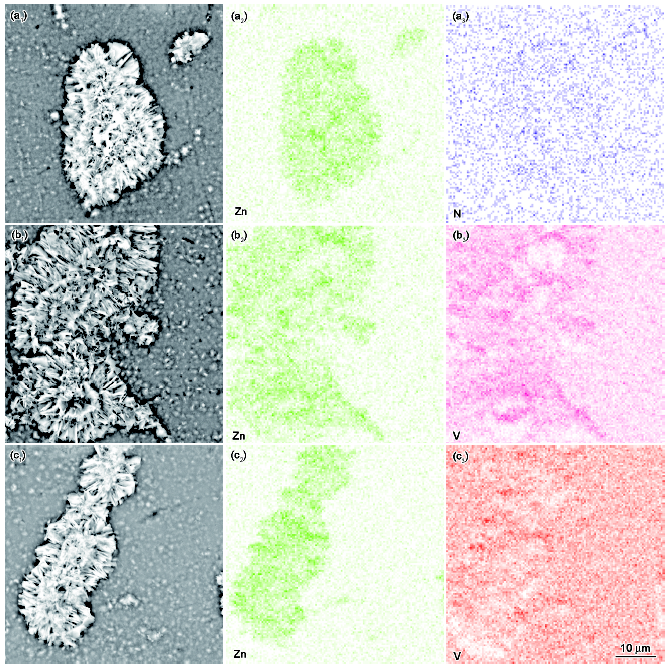
6061铝合金表面原位制备的ZnAl-LDHs-NO3层的SEM像及Zn、N元素EDS面扫描图如图3a1~a3所示。从图3a1可见,铝合金表面的ZnAl-LDHs-NO3层分布并不均匀,在某些区域呈云朵状聚集较多;ZnAl-LDHs-NO3层呈片状垂直于铝合金基体表面。从N元素的分布(图3a3)可以看出,整个6061铝合金表面布满了ZnAl-LDHs-NO3层。6061铝合金表面原位制备的ZnAl-LDHs-VO4层的SEM像及相应的EDS面扫描图如图3b1~b3所示。图3b1的ZnAl-LDHs-VO4的微观形貌特征与图3a1的ZnAl-LDHs-NO3层的微观形貌基本相同。ZnAl-LDHs-VO4层的EDS元素分布中明显含有V (图3b3),说明在Na3VO4溶液中,ZnAl-LDHs层发生了酸根离子交换反应,VO43-取代NO3-插入到层间形成ZnAl-LDHs-VO4层,这与文献[24,34]提到的ZnAl-LDHs中的NO3-可以与不同价态的钒酸根离子发生交换相一致。6061铝合金表面原位制备的ZnAl-LDHs-VO3层的SEM像及Zn、V元素EDS面扫描图如图3c1~c3所示。图3c1的ZnAl-LDHs-VO3层的微观结构与ZnAl-LDHs-NO3层类似,在铝合金表面的部分区域出现富集现象;同时图3c3中的V元素分布也说明在NaVO3溶液中浸泡时,ZnAl-LDHs-NO3层间的NO3-和溶液中的VO3-发生离子交换反应,转化成ZnAl-LDHs-VO3层。
图3 6061铝合金表面不同ZnAl-LDHs层的SEM像及其相应的EDS面扫描图
Fig.3 SEM images (a1~c1) and related EDS maps (a2~c2, a3~c3) of ZnAl-LDHs-NO3 (a1~a3), ZnAl-LDHs-VO4 (b1~b3) and ZnAl-LDHs-VO3 (c1~c3) films on the 6061 Al alloy surface
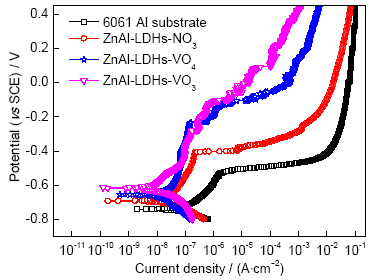
6061铝合金基体及表面不同ZnAl-LDHs层在3.5%NaCl溶液中的极化曲线如图4所示,其腐蚀电位(Ecorr)、腐蚀电流(Icorr)及点蚀电位(Ep)等电化学参数如表1所示。与6061铝合金基体相比,ZnAl-LDHs层能明显降低铝合金的Icorr,特别是ZnAl-LDHs-VO3层的Icorr约为铝合金基体的1/20,同时ZnAl-LDHs层能提高铝合金的Ecorr和Ep,这表明ZnAl-LDHs层能增强铝合金的耐腐蚀性能,可用作铝合金的防腐蚀保护。在3种ZnAl-LDHs层中,ZnAl-LDHs-VO3层具有最小的Icorr (1.40×10-8 A/cm2),较高的Ecorr (-0.615 V)以及最高的EP (-0.150 V),说明在这3种含不同酸根的ZnAl-LDHs层中,ZnAl-LDHs-VO3层的耐腐蚀性最好,这是由于VO3-作为缓蚀剂可以更好地抑制腐蚀反应的进行[28]。
图4 6061铝合金基体及不同ZnAl-LDHs层在3.5%NaCl溶液中的极化曲线
Fig.4 Polarization curves of the 6061 Al substrate and different ZnAl-LDHs films immersed in 3.5%NaCl solution
表1 6061铝合金基体及不同ZnAl-LDHs层的电化学参数
Table 1 Electrochemical parameters of the 6061 Al substrate and different ZnAl-LDHs films
6061铝合金基体及表面不同ZnAl-LDHs层经极化腐蚀(-0.8~1.0 V)后的表面形貌如图5所示。在相同的极化腐蚀条件下,不同ZnAl-LDHs层的腐蚀形貌明显不同。其中不含ZnAl-LDHs层的6061铝合金基体被腐蚀的程度最严重,其裸露的反应面全部被腐蚀(图5a);含ZnAl-LDHs-NO3层的铝合金被腐蚀的程度次之,腐蚀反应区域内出现大量的点蚀坑,点蚀坑的面积约占整个反应面的一半(图5b);含ZnAl-LDHs-VO4和ZnAl-LDHs-VO3层的铝合金表面的点蚀坑较少(图5c和d),其中ZnAl-LDHs-VO3层表面的点蚀坑最少,大部分反应面未被腐蚀(图5d)。表明ZnAl-LDHs-VO3层的耐腐蚀性能最佳,发生点蚀的几率较小。图5中A、B、C和D区域的三维腐蚀形貌如图6所示。可见,铝合金基体整个腐蚀区的深度约为12 μm (图6a),含ZnAl-LDHs-NO3层(图6b)、ZnAl-LDHs-VO4层(图6c)和ZnAl-LDHs-VO3层(图6d)的铝合金点蚀坑深度分别约为48、54和88 μm,点蚀坑深度依次增加,与图5所示点蚀坑的密度正好相反,这是因为当点蚀坑的密度较小时,腐蚀反应主要发生在少数的几个点蚀坑内,造成点蚀坑的深度较大。
图5 6061铝合金基体及表面不同ZnAl-LDHs层的极化腐蚀形貌
Fig.5 Corrosion morphologies of 6061 Al substrate (a), ZnAl-LDHs-NO3 (b), ZnAl-LDHs-VO4 (c) and ZnAl-LDHs-VO3 (d) films
图6 6061铝合金基体及表面不同ZnAl-LDHs层极化腐蚀后的三维形貌
Fig.6 3D corrosion morphologies of 6061 Al substrate (a), ZnAl-LDHs-NO3 (b), ZnAl-LDHs-VO4 (c) and ZnAl-LDHs-VO3 (d) films corresponding to areas A~D in
6061铝合金基体及不同ZnAl-LDHs层腐蚀形貌的SEM像如图7所示,各微区的EDS元素含量分析列于表2中。图7a中铝合金基体的腐蚀形貌呈现龟裂状和点蚀坑,各点蚀坑已经连通到一起。A1点的O含量大约是Al含量的3倍,说明龟裂状腐蚀产物主要是Al(OH)3,A2点的O含量和Al含量差不多,说明该区域主要为Al2O3[35,36]。图7b中点蚀坑边的腐蚀产物呈龟裂状,B1点的O含量远高于Al,且N元素含量较高,说明表面LDHs层中的NO3-参与了腐蚀产物的形成。图7c未腐蚀区域C2点含有少量V和Cl,说明铝合金表面的LDHs层将Cl-容纳到层间。图7d腐蚀形貌主要为点蚀,腐蚀区域D1含有少量V,V也形成了腐蚀产物,未腐蚀的云状区域D2点V含量较高,说明未腐蚀区域仍旧保持良好的耐蚀性。
表2
Table 2 EDS elemental compositions of the ZnAl-LDHs films after the polarization test at the positions indicated in
图7 6061铝合金基体及表面不同ZnAl-LDHs层极化腐蚀后的SEM像
Fig.7 SEM images of 6061 Al substrate (a), ZnAl-LDHs-NO3 (b), ZnAl-LDHs-VO4 (c) and ZnAl-LDHs-VO3 (d) films after the polarization test
6061铝合金中的第二相(如Mg2Si相和Al-Fe-Si相)与铝合金基体间存在电位差,在含Cl-环境中易发生点蚀[37,38],随着腐蚀反应的进行,整个铝合金基体被全部腐蚀。当铝合金表面含ZnAl-LDHs层时,致密的ZnAl-LDHs无机物涂层可以隔离腐蚀液中的Cl-与铝合金基体的直接接触,阻碍腐蚀反应的进行;同时ZnAl-LDHs层间对Cl-具有容纳性,当Cl-穿越ZnAl-LDHs层时,可以与ZnAl-LDHs层的酸根离子发生交换被容纳在ZnAl-LDHs层间,从而进一步防止Cl-与铝合金基体的接触[11,39];另外当Cl-与ZnAl-LDHs-VO3层间的VO3-发生交换时,会产生缓蚀剂(VO3-),可以进一步抑制腐蚀反应的进行,因此ZnAl-LDHs-VO3层的防腐蚀效果最好。
含不同ZnAl-LDHs层的6061铝合金及其基体在3.5%NaCl溶液中的EIS及其等效电路如图8所示。图8a所示的Bode图显示6061铝合金基体、ZnAl-LDHs-NO3层、ZnAl-LDHs-VO4及ZnAl-LDHs-VO3层在低频时的最大阻抗模分别为8.88×103、8.46×104、9.21×105和1.29×106 Ω ? cm2,含ZnAl-LDHs-NO3层的阻抗远大于铝合金基体。图8b、c的Bode图和Nyquist图显示在低频区(10-2~10-1 Hz)和中频区(10-1~103 Hz),不同LDHs层的阻抗谱出现2个时间常数。在中频区,3种ZnAl-LDHs层的阻抗谱相似,且时间常数向低频区移动;在低频区,ZnAl-LDHs-NO3与铝合金基体的阻抗谱相似,ZnAl-LDHs-VO4与ZnAl-LDHs-VO3的阻抗谱相似。这说明中频区的时间常数是由于表面存在的LDHs层导致,低频区的时间常数是电荷转移过程的双电层导致的。对于铝合金基体来说,这2个时间常数是由于铝合金表面的氧化膜以及电荷转移过程的双电层导致。
图8 6061铝合金基体和表面不同ZnAl-LDHs层的EIS及其等效电路图
Fig.8 Bode plots (a, b) and Nyquist plot (c) of 6061 Al substrate and different ZnAl-LDHs films and equivalent circuit (d) for modeling impedance data (CPELDHs—LDHs films capacitance; RLDHs—LDHs film resistance; CPEdl—double layer capacitance; Rct—charge transfer resistance, Rsol—solution resistance of electrolyte)
因此,含不同LDHs层的6061铝合金的EIS可用图8d所示的等效电路图来解释,其中Rsol表示电解质的溶液电阻;CPEdl表示电极的双电层电容;Rct表示ZnAl-LDHs层/溶液接触面的传递电阻;CPELDHs和RLDHs分别表示LDHs层引起的电阻和电容。由于存在弥散效应,在模拟时一般用常相位角元件(CPE)代替电路图中的等效电容,其阻抗为ZCPE=[Y(jω)n]-1(其中,Y为CPE常数,ω为频率,n为CPE指数)。其中0≤n≤1,当n=1时,ZCPE表示等效电容C;当n=0时,ZCPE表示等效电阻R;n的大小与样品表面有关,其表面的均匀度、缺陷及附着的氧化膜等都对n有影响。根据图8d所示的等效电路图对不同ZnAl-LDHs层的EIS进行拟合,所得拟合结果列在表3中。与腐蚀速率有关的电化学参数为极化电阻(Rp=Rct+RLDHs),6061铝合金基体、ZnAl-LDHs-NO3层、ZnAl-LDHs-VO4及ZnAl-LDHs-VO3层的Rp分别为9.86×103、9.28×104、1.37×106及5.67×106 Ω ? cm2,其中ZnAl-LDHs-VO3层的Rp最大,ZnAl-LDHs层能明显增强铝合金的抗腐蚀性,这与图4的极化腐蚀数据的分析结果一致。
表3 6061铝合金基体和表面不同ZnAl-LDHs层在3.5%NaCl溶液中的EIS等效电路拟合结果
Table 3 Fitting parameters of the equivalent circuit of 6061 Al substrate and different ZnAl-LDHs films in 3.5%NaCl solution
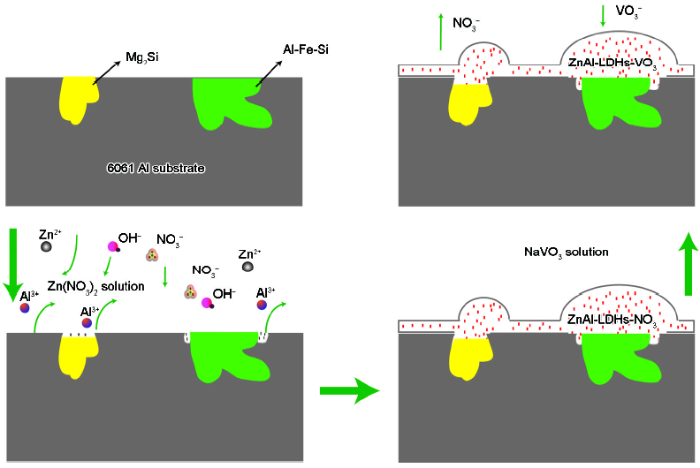
形成ZnAl-LDHs-NO3层时,6061铝合金首先发生电化学腐蚀,向溶液中提供Al3+,其反应过程如图9所示。6061铝合金中存在Mg2Si和Al-Fe-Si等第二相,其与铝合金基体存在电位差。Al-Fe-Si相的电位约为-0.2 V,比铝合金基体的电位高,作为阴极;Mg2Si相的电位约为-1.2 V,比铝合金基体的电位低,作为阳极[6,35]。因此在pH=7的Zn(NO3)2溶液中第二相区域形成微电偶,导致Al-Fe-Si相周围的铝合金基体比其它区域优先溶解,发生阳极反应(1);在LDHs层的形成过程中可以观察到样品表面有气泡产生,所以Al-Fe-Si相上主要发生阴极反应(2);样品表面的阴极反应造成微区pH值升高,溶液中的Zn2+发生反应(3);综上所述,ZnAl-LDHs-NO3层的生成可以用反应方程(4)表示[40,41]。6061铝合金表面的其它区域同样发生着Al溶解和LDHs层的生成过程,Al-Fe-Si相附近的Al3+浓度和pH值较高,该区域的H2O、OH-、Al3+和Zn2+优先反应,因此在Al-Fe-Si相区域形成的ZnAl-LDHs-NO3层较厚,如图3a1和图9所示。同时又因为该区域的pH值较高,并且溶液中的Zn2+浓度较高,导致部分Zn(OH)2沉淀,造成Zn的富集,如图3a2所示。溶度积常数(Ksp)与反应的Gibbs自由能(ΔrGmΘ)的关系式为ΔrGmΘ=-RTlnKsp,其中R为摩尔气体常数,T为热力学温度。Ksp越小,越容易形成沉淀。Mg(OH)2的溶度积(常温下为5.0×10-12)远大于Zn(OH)2的溶度积(常温下为1.0×10-17),即相同条件下,首先产生Zn(OH)2沉淀;又因为溶解在溶液中的Mg2+含量远小于Zn2+含量,因此没有发现MgAl-LDHs形成。
图9 6061铝合金表面ZnAl-LDHs层的制备过程图
Fig.9 Preparation process diagram of the ZnAl-LDHs film on 6061 Al alloy surface
ZnAl-LDHs-VO3层的形成是利用LDHs具有离子交换性的特点,LDHs层间的阴离子能够与电解液中的酸根离子发生离子交换反应。ZnAl-LDHs-NO3层中原有的NO3-容易被其它阴离子置换出来,该交换反应如式(5),缓蚀剂VO3-进入ZnAl-LDHs层间,如图3c3和图9所示。
前述极化曲线和EIS的分析结果显示,ZnAl-LDHs-VO3层能明显提升铝合金的耐腐蚀性。这是由于致密的ZnAl-LDHs-VO3层能够隔离Cl-与铝合金的直接接触;Cl-能够与ZnAl-LDHs-VO3层间VO3-发生离子交换,如反应(6)所示,并与带正电的层板成键,将Cl-容纳到LDHs层中,限制了Cl-向基体的扩散,延长Cl-到达基体表面的时间;ZnAl-LDHs-VO3层释放出来的VO3-具有钝化作用,腐蚀区域可以进行自我修复,再次形成致密的钝化膜,从而抑制铝合金腐蚀,如式(7)所示。
(1) 采用原位生长的方法,在6061铝合金表面成功制备了ZnAl-LDHs-NO3层,然后通过离子交换制备了ZnAl-LDHs-VO4和ZnAl-LDHs-VO3层。ZnAl-LDHs层呈片状垂直于基体生长,LDHs层的形貌较为致密,能够完全覆盖于铝合金表面。
(2) ZnAl-LDHs层能够明显增强6061铝合金的耐腐蚀性,可用于铝合金表面的防腐蚀保护,所研究的3种ZnAl-LDHs层中,ZnAl-LDHs-VO3的耐腐蚀性最高。其耐腐蚀机理可解释为:致密的ZnAl-LDHs无机物涂层可以隔离腐蚀液与铝合金基体的接触,阻碍铝合金基体腐蚀反应的进行;ZnAl-LDHs层间对Cl-具有容纳性,当Cl-穿越ZnAl-LDHs层时,可以与ZnAl-LDHs层间的酸根离子发生交换被吸附在ZnAl-LDHs层间,进一步阻止Cl-与铝合金基体的接触;另外当Cl-与ZnAl-LDHs-VO3层间的VO3-发生交换时,会产生缓蚀剂(VO3-),抑制铝合金基体的腐蚀反应。
 , 李纯民
, 李纯民
1 实验方法
2 实验结果
2.1 ZnAl-LDHs层的结构与形貌
2.2 ZnAl-LDHs层的电化学腐蚀行为
Specimen
Ecorr / V
Icorr / (μAcm-2)
Ep / V
6061 Al substrate
-0.758
0.315
-0.538
ZnAl-LDHs-NO3
-0.692
0.057
-0.405
ZnAl-LDHs-VO4
-0.655
0.031
-0.233
ZnAl-LDHs-VO3
-0.615
0.014
-0.150


Area
O
Al
Cl
Zn
N
V
A1
74.88
24.27
0.85
-
-
-
A2
51.10
48.90
-
-
-
-
B1
75.56
13.82
-
-
10.62
-
B2
45.21
43.98
-
0.74
10.07
-
C1
74.46
24.56
0.98
-
-
-
C2
50.57
42.49
0.94
4.25
-
1.76
D1
52.25
47.49
-
-
-
0.39
D2
57.71
25.14
0.71
12.39
-
4.05


Specimen
CPELDHs / (Ω-1cm-2
RLDHs
Ωcm2
CPEdl / (Ω-1cm-2
Rct
Ωcm2
Y1
n1
Y2
n2
6061 Al substrate
1.34×10-5
0.25
9.01×100
5.37×10-6
0.85
9.86×103
ZnAl-LDH-NO3
4.25×10-6
0.97
3.41×102
4.25×10-6
0.87
9.28×104
ZnAl-LDH-VO4
3.59×10-6
0.77
1.27×103
4.33×10-6
0.91
1.37×106
ZnAl-LDH-VO3
4.39×10-6
0.76
1.25×103
4.04×10-6
0.91
5.67×106
3 分析与讨论
3.1 ZnAl-LDHs层的形成过程
3.2 ZnAl-LDHs层的耐腐蚀机理
4 结论
来源--金属学报






 沪公网安备31011202020290号
沪公网安备31011202020290号
