分享:600℃ NaCl盐雾环境下GH4169合金的腐蚀行为
张伟东1, 崔宇 ,2, 刘莉
,2, 刘莉 ,1, 王文泉1, 刘叡1, 李蕊1, 王福会1
,1, 王文泉1, 刘叡1, 李蕊1, 王福会1
1.
2.
利用氧化动力学测试,结合微观表征技术,从腐蚀动力学、腐蚀层相组成和组织结构等方面,研究了GH4169合金在600℃的NaCl盐雾环境中的腐蚀行为。研究表明,GH4169合金在NaCl盐雾和固态NaCl + 含O2水蒸汽环境下的腐蚀增重均明显增加,且后者的腐蚀速率显著大于前者。GH4169合金在NaCl盐雾环境下的腐蚀产物主要为Cr2O3、Fe2O3、NiFe2O4和NaNbO3,其腐蚀层较为致密,且氯在内腐蚀层中富集。在NaCl盐雾环境下,腐蚀初期GH4169合金以氧化和氯的活性氧化机理共同作用加速腐蚀,随着NaCl沉积量的增加合金腐蚀逐渐变为以氯的活性氧化机制为主的加速腐蚀。此外,对GH4169合金的主要元素及其氧化物在中温NaCl盐雾环境下的反应敏感性进行了计算分析,结果表明,NaCl盐雾环境下GH4169合金内各元素对氯活化腐蚀敏感性的排序依次为:Ti > Al > Nb、Cr > Fe >Mo、Ni,合金氧化物对环境的敏感性顺序为:TiO2 > MoO2 > Cr2O3(Nb2O5) > Fe2O3 > Al2O3 > NiO。
关键词:
随着我国海洋的开发及海防事业的蓬勃发展,沿海服役航空发动机的高温腐蚀问题日益突出。航空发动机由于服役于海洋环境,在其运行期间遭受到海洋高盐(NaCl)、高湿(H2O)等腐蚀性气氛和较高工作温度(300~700℃)的复杂耦合作用,发动机叶盘和叶片的腐蚀问题都极为严重,极大地缩短了发动机在海洋环境下的使用寿命[1~6]。因此,明晰发动机叶盘和叶片用材的高温腐蚀行为机制至关重要。
针对合金在500~700℃含氯固态盐中的腐蚀行为,Crabke等[7]建立了固态NaCl盐膜中氯的活性氧化(Cl active oxidation)腐蚀机制[7],认为氯存在于氧化膜之下,优先与合金基体反应,通过形成过渡的氯化物,而后再与氧反应转变成氧化物。在500~700℃的固态NaCl盐膜+水蒸汽协同作用下,纯Fe[6]、纯Cr[4]、Fe-Cr合金[6]、马氏体不锈钢[3]则存在反常腐蚀现象,即Cr含量越高,腐蚀速率越快。Liu等[8]和Tang等[9]在中温NaCl盐膜+水蒸汽环境下利用电偶腐蚀测量技术证实,合金腐蚀的过程中存在电化学反应,且同时存在化学-电化学交互作用[10,11]。而后国外研究团队[12,13]对此类腐蚀问题也进行了深入研究,但是针对金属材料在此类服役环境下的实际耐蚀能力评估存在争议。现有评价体系中环境模拟主要采用样品表面沉积固态盐膜、恒温控制结合外加水蒸汽输入的方法考核。但现阶段航发集团已制定严格的维护保养规范,发动机定期清洗,材料表面难以沉积大量NaCl固态盐膜。因此,前期模拟环境下的研究结果已不能满足对目前实际服役环境下材料耐蚀能力评估的需求。
目前涉海用飞机发动机的服役环境主要是含盐湿空气下的中高温腐蚀环境。海洋气氛主要由大量微小的NaCl颗粒和水蒸汽混合组成,随发动机运转被吸入压气机内部,并聚集在前端转子区域(300~700℃的工作温度)。最新研究结果[14]显示,NaCl含量及沉积方式对材料腐蚀行为具有显著影响。Fe-20Cr (质量分数,%)合金在NaCl盐雾和固态NaCl盐膜+水蒸汽协同作用下腐蚀20 h的腐蚀增重结果相近,这主要是因为在2种环境下Fe-20Cr合金都无法在表面形成连续Cr2O3膜,表面形成大量的Fe的氧化物导致腐蚀增重结果相近。然而,对Ti60合金的研究[15]则显示2种NaCl沉积环境结果相差显著,钛合金在盐雾环境下腐蚀20 h后的增重远远小于其在固态NaCl盐膜+水蒸汽环境下的腐蚀增重。Ti60合金在600℃ NaCl盐雾环境下腐蚀后,其表面形成相对致密且连续的TiO2氧化层,从而延缓了氯的腐蚀作用。由此可见,不同材料在更接近于发动机实际服役条件的盐雾环境和传统固态沉积盐环境下的中温腐蚀行为差异较大。
GH4169作为广泛应用于飞机发动机的高温合金,其在700℃以下具有较高的屈服强度和韧性及良好的耐腐蚀性能,可应用于发动机压气机转子叶片,其在服役过程中必然会面临中、高温盐雾腐蚀问题[16,17]。早期,Wang等[5]针对K38G合金(K38G为第一代耐蚀高温合金,GH4169为第二代耐蚀高温合金[18])在固态NaCl盐膜+水蒸汽中温环境下的腐蚀行为进行了研究,结果显示,K38G合金在此环境下的腐蚀速率显著高于单一O2、水蒸汽、单一固态盐环境。在NaCl盐膜+水蒸汽中温服役环境下,K38G合金中主要是Cr的氧化物与NaCl发生化学反应,导致氧化膜不再具有保护性,引发合金的严重腐蚀。其中,Cr对此环境敏感性很高,而其他合金元素对此环境敏感性尚未见系统性的研究报道。此外,Yu等[19]针对GH4169合金的高低温盐水循环下的腐蚀行为研究发现,GH4169合金除了Cr的氧化层不能稳定维持保护能力外,合金内其他元素对环境的敏感性也会进一步影响合金的耐蚀能力。但目前针对GH4169合金在中温(300~600℃)含NaCl环境下的腐蚀行为研究甚少,更未开展针对其在中温盐雾环境下腐蚀行为的系统研究。GH4169合金中主要元素在该复杂环境下的反应敏感性尚不清晰,需要开展深入研究。
综上,本工作选择涉海航空发动机服役合金GH4169作为研究对象,深入开展该合金在600℃下NaCl盐雾环境中的腐蚀行为研究。通过与相同温度下无盐(O2、含O2水蒸汽)和固态NaCl盐膜+含O2水蒸汽环境下的腐蚀行为对比,阐明该合金在不同模拟环境下的腐蚀动力学规律、腐蚀产物形貌、成分以及结构,并由此深入讨论GH4169合金在中温盐雾环境下的腐蚀机理及合金中的各元素对盐雾环境的敏感性序列,为涉海航空发动机高温合金的设计提供理论数据和参考。
1 实验方法
实验所用材料为国产发动机上实现大规模应用的GH4169高温合金,其名义成分(质量分数,%)为:C 0.045,Cr 19.09,Mo 3.25,Al 0.88,Ti 0.83,Fe 18.0,Nb + Ta 5.08,B 0.05,Ni余量。将GH4169合金加工成15 mm × 10 mm × 2 mm的片状样品,并在样品正下方2 mm处线切割直径为1.5 mm的孔用以悬挂。样品经过200~800号砂纸水磨,进行倒角、倒边处理,最终放置于酒精-丙酮溶液中进行超声清洗,而后冷风吹干,放入干燥器中备用。
本工作模拟了4种腐蚀环境:NaCl盐雾、固态NaCl盐膜通水蒸汽和O2 (简称固态NaCl + 含O2水蒸汽)、含O2水蒸汽和纯O2 (后3种模拟环境为对比实验),实验温度为(600 ± 2)℃。NaCl盐雾环境模拟装置如图1a所示,该装置由加热系统、通气装置、储水装置和超声雾化器共同组成,具体实验参数见文献[15]。其中实验温度恒定控制在600℃,盐雾雾化温度为75℃,水蒸汽含量控制为30.8%,载气(O2)流速控制为310 mL/min。3种对比实验具体参数如下。(1) 固态NaCl + 含O2水蒸汽实验:用毛刷在预热(210℃)的实验样品表面涂覆饱和NaCl水溶液,沉积固态NaCl盐膜,沉积量约为4 mg/cm2;实验装置由加热系统、通气装置和控温系统组成(图1b),载气(O2)流速为310 mL/min。(2) 含O2水蒸汽实验:水蒸汽含量控制为30.8%,载气(O2)流速为310 mL/min。(3) 纯O2实验:载气(O2)流速为310 mL/min (选择纯O2作为载气是为了在实验室环境下保持实验的稳定性[15])。
图1

图1 中温NaCl盐雾和固态NaCl + 含O2水蒸汽腐蚀模拟装置示意图
Fig.1 Schematics of NaCl solution spray environment (a) and the furnace system with the traditional solid NaCl in wet O2 environment (b)
采用Sartorius电子天平(测量精度为0.00001 g)对腐蚀样品进行称重,绘制腐蚀增重曲线。采用Inspect F50扫描电子显微镜(SEM)和Finder1000能谱仪(EDS)对腐蚀产物形貌及成分进行半定量分析。利用EPMA-1610电子探针(EPMA)和X'Pertpro型X射线衍射仪(XRD,实验测试参数如下:采用旋转Cu 靶,工作电流为40 mA,工作电压为40 kV,扫描角度为20°~90°,扫描速率为10°/min,步长为0.02°)对腐蚀产物成分进行分析。采用HE-LIOS-600i型聚焦离子束(FIB)制备TEM样品,并用JEM 2100透射电镜(TEM)对腐蚀产物微观结构进行深入表征。针对NaCl盐雾、O2和含O2水蒸汽腐蚀样品采用掠射角X射线衍射方法(GIXRD)进行分析;由于固态NaCl + 含O2水蒸汽样品腐蚀产物膜厚且腐蚀产物疏松,将腐蚀产物剥离后进行粉末收集,并进行直角XRD分析。
2 实验结果
2.1 腐蚀动力学
图2为GH4169合金在4种中温腐蚀环境下(纯O2、含O2水蒸汽、NaCl盐雾和固态NaCl + 含O2水蒸汽环境)腐蚀20 h的动力学曲线。从图可见,样品在纯O2和含O2水蒸汽环境下腐蚀增重甚微,且2者在腐蚀动力学上的差异不明显。样品在含NaCl环境下的腐蚀增重较无NaCl环境明显增加,在固态NaCl + 含O2水蒸汽环境下腐蚀20 h增重量为(7.32 ± 0.35) mg/cm2,且腐蚀前期增重较快,后期腐蚀增重趋于缓慢;样品在NaCl盐雾环境下腐蚀20 h后的增重为(0.53 ± 0.06) mg/cm2,腐蚀增重变化较平缓。
图2
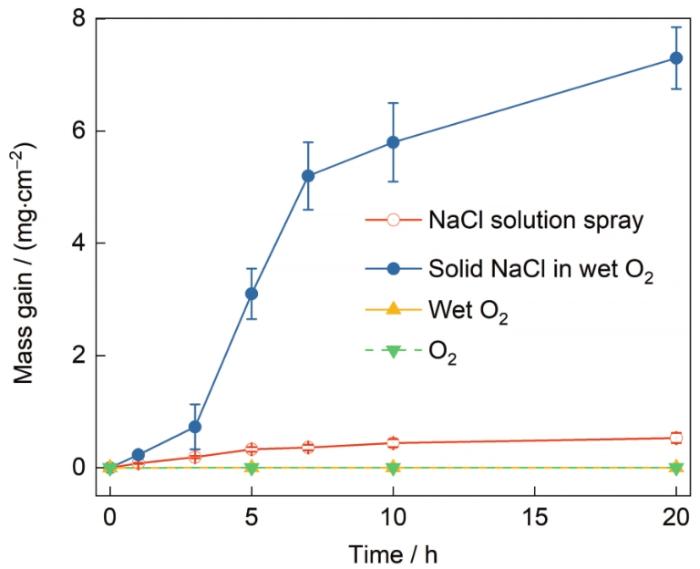
图2 GH4169合金在600℃的纯O2、含O2水蒸汽、固态NaCl + 含O2水蒸汽和NaCl盐雾环境下腐蚀 20 h的腐蚀动力学曲线
Fig.2 Mass gain curves of GH4169 exposed in pure O2, wet O2, solid NaCl in wet O2, and NaCl solution sprayenvironments at 600oC for 20 h
2.2 腐蚀产物形貌
图3为样品分别在固态NaCl + 含O2水蒸汽和NaCl盐雾环境下放置5 min后的表面SEM像。由于腐蚀时间较短,因此该结果主要反映了2种模拟环境下NaCl在样品表面的沉积状态。图3a表明,固态NaCl + 含O2水蒸汽环境下样品表面涂覆的NaCl盐膜较厚,颗粒密集。图3b表明,NaCl盐雾在5 min内以颗粒状沉积在样品表面,沉积量少并且分布不均匀。样品表面已有氧化物初步形成的特征。2种模拟环境下盐的沉积量和沉积方式显著不同。
图3

图3 GH4169合金在600℃的固态NaCl + 含O2水蒸汽和NaCl盐雾环境服役5 min后表面SEM像
Fig.3 SEM images of GH4169 alloy exposed in solid NaCl in wet O2 (a) and NaCl solution spray (b) environments at 600oC for 5 min
GH4169合金在4种中温环境下(纯O2、含O2水蒸汽、固态NaCl + 含O2水蒸汽和NaCl盐雾环境)腐蚀20 h后的表面SEM像如图4所示。结果表明,在纯O2 (图4a)和含O2水蒸汽(图4b)环境中腐蚀20 h后,样品表面均存在清晰可见的划痕,局部放大图像(4a和b插图)发现样品表面有颗粒状的腐蚀产物,且含O2水蒸汽环境中生成的腐蚀产物更多更大。EDS结果(表1)显示此颗粒主要含有Cr和O元素。由图4c可见,样品经固态NaCl + 含O2水蒸汽腐蚀20 h后,表面的腐蚀产物较疏松,呈现“菜花”状。进一步放大图像(图4c插图)发现,腐蚀产物由不致密的颗粒团簇堆积而成。EDS结果表明,该腐蚀产物主要由Fe、Cr和O元素构成(表1)。由图4d可见,样品经NaCl盐雾腐蚀20 h后,表面腐蚀产物由少量凸出状的大尺寸颗粒和致密片层状腐蚀产物组成。放大片层区域(图4d插图)显示该腐蚀膜较完整致密、无明显裂纹。EDS初步分析发现,凸出状的大尺寸颗粒产物内主要含有Na、Nb和O元素;致密片层状腐蚀产物主要由Ni、Fe、Cr和O元素构成(表1)。
图4

图4 GH4169合金在600℃纯O2、含O2水蒸汽、固态NaCl + 含O2水蒸汽和NaCl盐雾环境下腐蚀20 h后的表面SEM像
Fig.4 SEM images of GH4169 alloy exposed in pure O2 (a), wet O2 (b), solid NaCl in wet O2 (c), and NaCl solution spray (d) environments at 600oC for 20 h (Insets show the corresponding high magnified images)
表1 图4中各点的EDS结果 (mass fraction / %)
Table 1
| Point | Cr | Ni | Na | Al | Ti | Fe | Nb | O |
|---|---|---|---|---|---|---|---|---|
| 1 | 35.54 | 2.13 | - | - | 0.02 | 0.05 | 0.03 | 62.23 |
| 2 | 29.83 | 1.35 | - | 0.03 | 0.03 | 1.03 | 0.06 | 67.67 |
| 3 | 3.37 | 3.10 | 0.07 | 0.02 | 0.04 | 59.93 | 0.10 | 33.37 |
| 4 | 2.31 | 1.42 | 22.25 | 0.02 | 0.95 | 1.07 | 23.14 | 49.91 |
| 5 | 15.61 | 15.58 | 1.82 | 0.73 | 0.65 | 10.53 | 2.71 | 52.37 |
GH4169合金在4种中温环境下腐蚀20 h后的截面SEM像如图5所示。由图5a和b可见,样品在纯O2和含O2水蒸汽环境下生成的腐蚀产物膜很薄,与表面形貌对应。由图5c可见,样品经固态NaCl + 含O2水蒸汽环境腐蚀20 h后,表面形成约70 μm厚的双层腐蚀产物膜,外腐蚀层存在大量裂纹和缺陷(约40 μm),内腐蚀产物层中存在大量孔洞(深度约30 μm)但相对致密,且合金样品存在较严重的内腐蚀现象。从图5d可以看出,在NaCl盐雾环境下腐蚀20 h后样品表面形成了约1.5 μm厚的连续腐蚀产物层,腐蚀产物层相对致密,没有明显的缺陷,未发现明显内腐蚀现象。
图5

图5 GH4169合金在600℃纯O2、含O2水蒸汽、固态NaCl + 含O2水蒸汽和NaCl盐雾环境腐蚀20 h后的截面SEM像
Fig.5 Cross-section SEM images of GH4169 alloy exposed in pure O2 (a), wet O2 (b), solid NaCl in wet O2 (c), and NaCl solution spray (d) environments at 600oC for 20 h
2.3 腐蚀产物的成分
GH4169合金在4种中温环境下腐蚀20 h后表面腐蚀产物的XRD谱如图6所示。纯O2和含O2水蒸汽2种环境下样品表面腐蚀产物衍射峰较少,主要为Cr2O3。样品在NaCl盐雾环境下腐蚀后,表面腐蚀产物衍射峰较多,除Cr2O3外,还存在Fe2O3、NiFe2O4和NaNbO3。固态NaCl + 含O2水蒸汽环境下的样品腐蚀产物衍射峰更为复杂,包括Cr2O3、NiO、NiCr2O4、Fe2O3、FeCr2O4、NaNbO3和Na2CrO4
图6
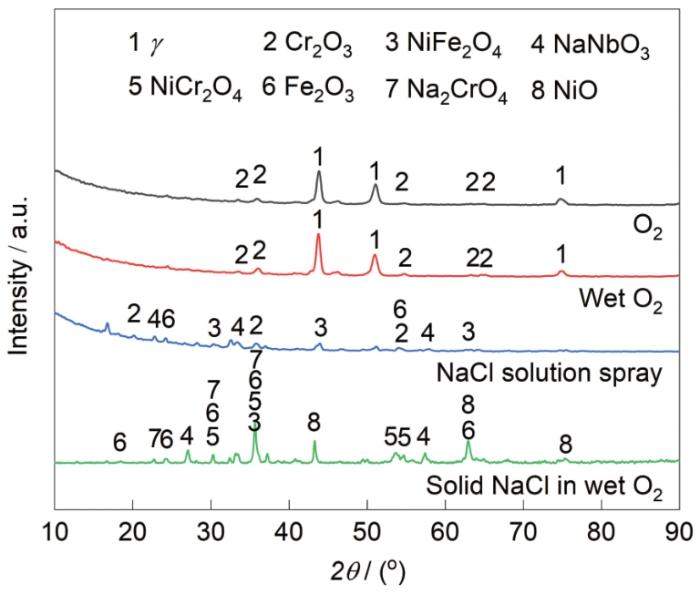
图6 GH4169合金在600℃纯O2、含O2水蒸汽、固态NaCl + 含O2水蒸汽和NaCl盐雾环境下腐蚀20 h的XRD谱
Fig.6 XRD spectra of GH4169 alloy exposed in pure O2, wet O2, solid NaCl in wet O2, and NaCl solution spray environments at 600oC for 20 h
图7为GH4169合金在固态NaCl + 含O2水蒸汽和NaCl盐雾环境腐蚀20 h后截面EPMA元素面分布图。可见,样品在固态NaCl + 含O2水蒸汽环境腐蚀后,产物外层Fe和Cr元素的富集较明显。Na、Al、Ti和Nb元素分布在腐蚀产物内层且远离基体的区域,而Ni和Mo元素在内腐蚀区出现富集现象,Cl元素在腐蚀产物层中分布不显著(图7a)。样品在NaCl盐雾环境腐蚀后,元素分布出现不同程度的变化。腐蚀层中Ni、Fe和Mo元素分布较为均匀,Ti、Al、Cr和Nb元素都有不同程度的富集,Na元素分布在腐蚀产物的外侧,Cl元素没有明显的分布规律(图7b)。
图7

图7 GH4169合金在600℃固态NaCl + 含O2水蒸汽和NaCl盐雾环境下腐蚀20 h后截面的EPMA元素面分布图
Fig.7 EPMA maps of the elemental distribution of the cross-section of GH4169 alloy exposed in solid NaCl in wet O2 (a) and NaCl solution spray (b) environments at 600oC for 20 h
图8为合金GH4169在中温NaCl盐雾长期(100 h)腐蚀后的腐蚀产物截面EPMA元素面分布图。与短期NaCl盐雾环境腐蚀的样品(图7b)相比,样品经长期的盐雾腐蚀后,表面形成了较厚的腐蚀产物层,并出现合金的内腐蚀现象,腐蚀层中元素分布也出现变化。长期腐蚀后样品腐蚀层中Ni在内腐蚀区域存在明显的富集现象,但只有少量分布在腐蚀产物外层。Cr少量分布于腐蚀层内侧,Fe较多分布在腐蚀层外层,且在合金内腐蚀区域存在明显的贫Fe和Cr现象。Ti和Al在腐蚀层中分布较广;Mo在腐蚀层中有很少分布,且在基体处有少量的富集。Na和Nb弥散分布在腐蚀层内,与短期盐雾环境相比其分布范围更大。同样,Cl元素在整个腐蚀区域都未发现富集,这与设备的测试精度有关。
图8
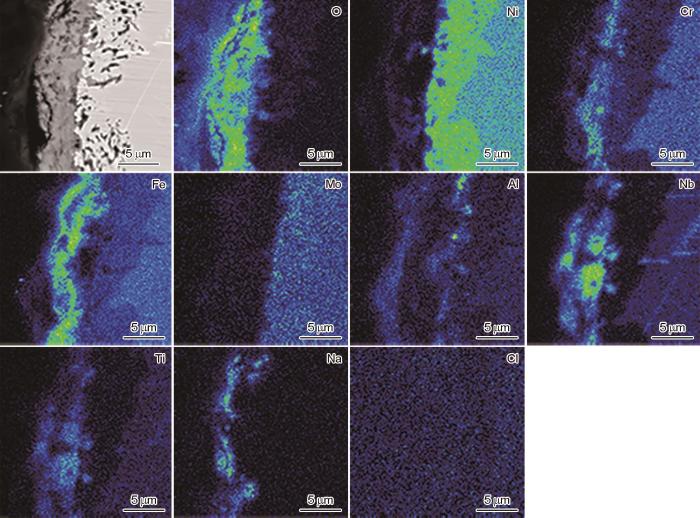
图8 GH4169合金在600℃的NaCl盐雾环境中腐蚀100 h后截面的EPMA元素面分布图
Fig.8 EPMA maps of the elemental distribution of the cross-section of GH4169 alloy exposed in NaCl solution spray environment at 600oC for 100 h
2.4 腐蚀产物的微观结构
图9为GH4169合金在中温NaCl盐雾环境腐蚀20 h后腐蚀产物膜的TEM像、选区电子衍射(SAED)花样和Cl元素线分布图。如图9a所示,样品经NaCl盐雾腐蚀20 h后,表面生成了含有许多纳米级孔洞的腐蚀层,虽然腐蚀层在微观上不致密但仍是连续的,并对合金基体具有一定的保护性。同样,不同腐蚀产物呈现出不同的形貌特征,因此对不同位置的腐蚀产物进行SAED分析。Spot 1为最外侧腐蚀产物,SAED分析表明其为FeNi2O4,此产物为尖晶石结构,从TEM形貌上可以看出其结构较致密。Spot 2为更靠近基体侧的腐蚀产物,其结构相对疏松,且内部存在孔洞。SAED分析结果为Fe2O3,这种疏松Fe2O3的生成可能与氯的活性氧化机制有关。Spot 3为内部腐蚀产物,其更靠近基体处生成,SAED结构表明其为Cr2O3,内部没有明显的缺陷结构。经分析Spot 4为NaNbO3,该腐蚀产物与Cr2O3生成位置相近。通过TEM-EDS线扫结果(图9b)证实在腐蚀产物膜中存在少量的氯,且主要在氧化膜/基体的界面处富集。可见,氯参与腐蚀的过程,但其含量较低,因此在EPMA结果中并没有明显表现出来。
图9
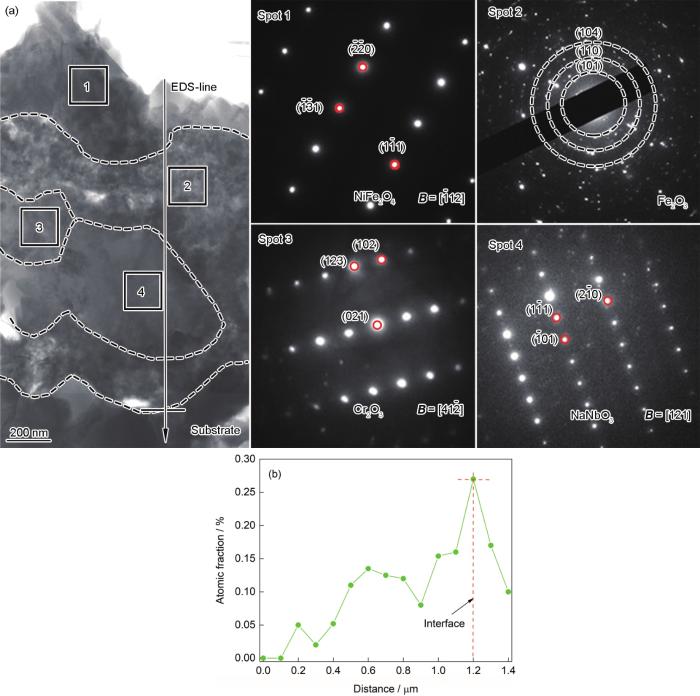
图9 GH4169合金在600℃下NaCl盐雾环境腐蚀20 h后腐蚀产物膜的TEM像、SAED花样及Cl元素线分布结果
Fig.9 TEM image and corresponding SAED patterns of the corrosion scale of GH4169 alloy exposed in NaCl solution spray at 600oC for 20 h (a), and Cl element distribution along the EDS-line in Fig.9a (b)
图10a~c为GH4169合金在固态NaCl + 含O2水蒸汽环境腐蚀20 h后内腐蚀区域的TEM像。由图10a可见,样品出现了内腐蚀产物区,且有明显孔洞和裂纹等缺陷。从局部放大图(图10b和c)可以看出,在晶界处存在优先内腐蚀的现象。Area 1为基体内相邻两晶粒的优先内腐蚀区域(图10b),经EDS分析,红点处成分(质量分数,%)为:Cl 0.41,Cr 15.64,Mo 0.21,Al 1.53,Ti 3.46,Fe 1.24,Nb 15.46,Ni 4.43,O 57.62。图10d为图10b的EDS面扫描结果(Area 1)。结合此区域EDS点扫描结果表明,Nb和Cr元素在内腐蚀区域优先富集,同时也发现Ti和Al元素在此区域的富集(合金中Ti和Al元素含量很低)。Fe和Ni元素主要分布在金属基体内,在内腐蚀区没有明显分布,可见这2种元素没有优先发生腐蚀。此外,Mo元素在整个区域没有明显的富集现象,这与EPMA结果(图7a)相吻合。Cl元素在晶界处有明显的富集现象,表明Cl会发生沿晶界的扩散行为,且Cl的优先扩散可能是腐蚀发生的前提条件。
图10
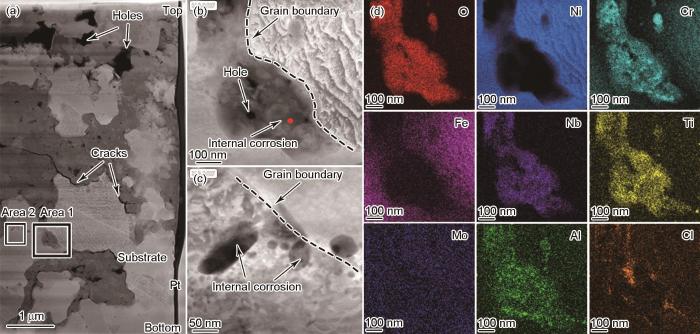
图10 GH4169合金在600℃固态NaCl + 含O2水蒸汽环境腐蚀 20 h后内腐蚀区域的TEM像及EDS结果
Fig.10 TEM image of internal corrosion scale of GH4169 alloy exposed in solid NaCl in wet O2 environment at 600oC for 20 h (a), and corresponding high magnified images of areas 1 (b) and 2 (c) in Fig.10a, respectively, and STEM-EDS result of Fig.10b (d)
3 分析讨论
3.1 GH4169合金在600℃ NaCl盐雾环境下的腐蚀机理
通常,含Cr合金在高温下形成的Cr2O3氧化膜对基体具有保护作用。GH4169合金在中温O2/含O2水蒸汽环境中腐蚀20 h后,表面形成连续、致密的Cr2O3层(图4~6),但致密的Cr2O3会与水蒸汽发生反应转化为挥发性的铬氢氧化物,例如CrO2(OH)2,此过程虽然发生的缓慢,但也会破坏氧化膜[20~24]。GH4169合金在中温NaCl盐雾和固态NaCl + 含O2水蒸汽环境中腐蚀程度更为明显,可见NaCl的存在显著加速了GH4169合金在600℃时的腐蚀速率,但2种环境下腐蚀行为却有着很大差异。
GH4169合金在固态NaCl + 含O2水蒸汽环境下,表面不能形成连续的保护性Cr2O3层,而是形成了疏松且复杂的腐蚀产物(Cr2O3、NiO、NiCr2O4、Fe2O3、FeCr2O4、NaNbO3和Na2CrO4等)。合金腐蚀增重明显,这与K38G合金的腐蚀结果[5]相类似,同样也发生了严重的内腐蚀行为。固态NaCl + 含O2水蒸汽环境下初始时NaCl沉积量高,氧化物与NaCl的化学反应快速且剧烈,因此形成的腐蚀产物疏松多孔(图5d),外界的O2、水蒸汽等更容易通过缺陷穿过氧化物层,促进基体金属腐蚀,并且在基体内发生内腐蚀。
GH4169合金在NaCl盐雾环境下腐蚀20 h后,表面形成了连续的腐蚀产物层,其主要成分为Fe2O3、NiFe2O4、Cr2O3和NaNbO3 (图6)。虽然形成的腐蚀产物层在样品腐蚀过程中有一定的阻挡作用,但对基体保护作用减弱,不能阻挡基体元素Fe和Ni的氧化。GH4169合金在2种NaCl环境下展现出不同的腐蚀行为,这与盐的沉积量与沉积方式有直接关系(图3)。NaCl盐雾环境下,NaCl颗粒逐渐沉积在样品表面。腐蚀初期的NaCl沉积量少并且分布不均匀(图3b),这导致在NaCl沉积处,优先发生氧化物与NaCl的化学反应,并引发氯的活性氧化(生成NaNbO3等);而没有NaCl沉积的区域,GH4169合金则发生经典氧化反应,会形成连续氧化物层。连续保护性氧化物膜的形成与破坏是经典氧化行为与氯的活性氧化竞争的结果[15]。这种腐蚀行为导致GH4169合金会形成相对致密且对腐蚀有一定阻碍作用的腐蚀产物层。但是,随着腐蚀时间延长到100 h (图8),GH4169合金在NaCl盐雾环境下腐蚀过程逐渐加速,也发生内腐蚀,这与氯的活性氧化加剧有直接关系[15]。从实验结果分析,GH4169合金在NaCl盐雾环境下的初期腐蚀行为是氯的活性氧化与经典氧化共同竞争的腐蚀机制;随着腐蚀时间延长,氯的活性氧化机制最终控制整个腐蚀过程。
通过上述分析发现,GH4169合金在固态NaCl + 含O2水蒸汽环境和NaCl盐雾环境均会引发氯的活性氧化腐蚀机理[7]。因此,根据本研究结果可对GH4169合金在NaCl盐雾环境的腐蚀机理推断如下。
GH4169合金在中温NaCl盐雾环境下首先发生氧化反应,最先形成Cr2O3、Nb2O5等氧化物,并形成连续氧化膜。而NaCl颗粒沉积处则会发生氧化物与NaCl、H2O、O2的反应:
反应(1)~(3)产生的HCl/Cl2在O2/氧化物层外表面高氯压的作用下,通过氧化物层向内传输,到达金属/氧化物界面(图9b)。在金属/氧化物界面处形成高氯分压,氯与合金中的金属元素M (M = Fe、Cr、Ni、Nb、Ti、Al、Mo)在高温下发生系列化学反应:
生成的各种金属氯化物具有较高的挥发性,将通过腐蚀层的孔洞等缺陷向外扩散。随着氯化物的向外扩散,相应区域的O2分压逐渐升高,金属氯化物与O2发生氧化反应形成疏松的复杂氧化物:
其中,反应(6)产生的Cl2会再次向金属/氧化物界面扩散,并与基体合金元素再次发生氯化反应,建立了完整的氯的活性氧化腐蚀机制[7]。GH4169合金在中温NaCl盐雾环境下首先发生的是氯的活性氧化与经典氧化机理共同竞争的腐蚀行为,腐蚀产物中有经典氧化形成的致密氧化物,也有活化氧化形成的疏松氧化物,但氧化物层整体连续,具有一定保护能力,这也是腐蚀相同时间后GH4169合金在NaCl盐雾环境下腐蚀速率远低于固态NaCl + 含O2水蒸汽环境的原因。但随着反应时间延长,NaCl沉积量越来越多,上述的氯的活性氧化机理最终控制GH4169合金的整个腐蚀过程。
3.2 GH4169合金对NaCl盐雾环境的敏感性
3.2.1 合金氧化物敏感性
高温环境下合金一般会生成氧化物层,如果环境中存在腐蚀性介质(NaCl、H2O),氧化物与介质发生化学反应的能力决定了氧化物层对合金的保护性[24~26]。通常,氧化物在腐蚀性介质中化学反应的标准Gibbs自由能是判断腐蚀反应发生难易的重要标准,即氧化物在该环境下的敏感性。本工作中无论是固态涂覆NaCl盐膜还是盐雾环境下沉积的NaCl颗粒,都是以固态形式沉积在样品表面(图3)。但有研究[26,27]表明,在NaCl与氧化物发生化学反应过程中,其可能会以气态形式参与反应,因此在计算化学反应标准Gibbs自由能时,反应方程中NaCl以气态进行处理。表2列出了GH4169合金理论上形成的氧化物在600℃ NaCl盐雾环境下各化学反应标准Gibbs自由能的计算结果(通过HSC Chemistry 5.11数据库计算)。结果表明,在600℃与NaCl化学反应的TiO2、MoO2和Cr2O3 Gibbs自由能皆为负值;Fe2O3和Al2O3为正值。标准Gibbs自由能越小,反应的趋势越大,即氧化物在该环境下的敏感性越强。根据理论计算结果,GH4169合金可形成的各氧化物与NaCl发生化学反应的趋势强弱顺序为TiO2 > MoO2 > Cr2O3 > Fe2O3 > Al2O3。从实验结果中确定生成了NaNbO3,表明在此环境中Nb2O5与NaCl发生了化学反应,并且Nb2O5在此环境下的敏感性较高(图9a)。因此,虽然不能清楚计算出Nb2O5与NaCl化学反应的具体Gibbs自由能 (各数据库内不含Nb2O5在600℃标准数据),但根据本工作结果可知Nb2O5与Cr2O3反应活性相近。在已有研究结果[14]中,Fe2O3可以与NaCl发生化学反应,但反应能力低于Cr2O3。而Al2O3与NaCl的化学反应未见报道,其为稳定性较强的氧化物。NiO与NaCl、H2O和O2在高温下很难形成NaNiO2,有报道[28]称其在此环境下的敏感性远低于Al2O3,因此NiO应该是在该环境下最稳定的氧化物。综上,在600℃ NaCl盐雾环境下GH4169合金可形成的氧化物中,TiO2、MoO2、Cr2O3和Nb2O5对此环境敏感性较高,属于活性氧化物;Fe2O3属于一般稳定性氧化物;Al2O3和NiO对此环境敏感性较低,属于惰性氧化物。
表2 相关化学反应在600℃时的标准Gibbs自由能
Table 2
| Reaction | ΔG0 / (kJ·mol-1) |
|---|---|
| 4NaCl (g) + O2 (g) + 2TiO2 = 2Na2TiO3 + 2Cl2 (g) | -133.57 |
| 4NaCl (g) + 2H2O (g) + TiO2 = 2Na2TiO3 + 4HCl (g) | -64.06 |
| 4NaCl (g) + 2Al2O3 + 2H2O (g) = 4NaAlO2 + 4HCl (g) | 280.4 |
| 4NaCl (g) + 2Al2O3 + O2 (g) = 4NaAlO2 + 2Cl2 (g) | 174.2 |
| 4NaCl (g) + 2Fe2O3 + O2 (g) = 4NaFeO2 + 2Cl2 (g) | 4 |
| 4NaCl (g) + 2Fe2O3 + 2H2O (g) = 4NaFeO2 + 4HCl (g) | 3.8 |
| 4NaCl (g) + Cr2O3 + 2H2O (g) + 3/2O2 (g) = 2Na2CrO4 + 4HCl (g) | -54.5 |
| 4NaCl (g) + Cr2O3 + 5/2O2 (g) = 2Na2CrO4 + 2Cl2 (g) | -54.4 |
| 4NaCl (g) + 4NiO + O2 + 2H2O = 4NaNiO2 + 4HCl (g) | - |
| 4NaCl (g) + 2Nb2O5 + O2 (g) = 4NaNbO3 + 2Cl2 (g) | - |
| 4NaCl (g) + 2H2O (g) + 2MoO2 + O2 (g) = 2Na2MoO4 + 4HCl (g) | -115.6 |
3.2.2 合金元素敏感性
前人[4,5,11~15]对中温固态NaCl膜 + 水蒸汽环境下的常用金属开展了大量的研究工作,发现不同合金元素在此环境的敏感性具有较大的差异。当GH4169合金在NaCl盐雾环境中发生腐蚀后,随着氯的活性氧化腐蚀机理的发生,使得Cl2/HCl传输到金属/氧化物界面,与合金元素发生化学反应(4)和(5)。此时认为GH4169合金中不同元素与氯反应难易程度(敏感性)与合金的耐蚀性能有直接关系。因此,根据本工作结果及相关机理对GH4169合金内各合金元素的耐中温氯敏感性进行深入分析。
根据HSC Chemistry 5.11数据库计算并绘制了GH4169合金主要元素在M-Cl-O体系600℃、 0.1 MPa压力下纯组分的相平衡图(以lg
图11

图11 M-Cl-O体系在600℃时以lgp
Fig.11 Equilibrium diagram of M-Cl-O system at 600oC with lgp
此外,由内腐蚀区域TEM像及EDS结果(图10)可知,内腐蚀区域腐蚀产物中存在大量孔隙,且在优先腐蚀的晶界处发现了Cl元素富集现象,可见Cl可以沿晶界快速传输[27~30]。GH4169合金内腐蚀现象的产生与内部结构有关,氯可以沿晶界等金属内缺陷快速传输,从而加剧合金内氯的活性氧化腐蚀。同样,内腐蚀的形成可能与合金内含有缺陷有关,O2和Cl2/HCl可以通过缺陷快速进入并与基体合金元素反应形成内腐蚀产物[31,32]。由此可见,合金内部的微观缺陷以及晶界是中温海洋环境下氯的快速传输通道,其对合金元素抵抗氯的腐蚀十分重要。
4 结论
(1) GH4169合金在NaCl盐雾环境下的腐蚀增重显著小于其在固态NaCl + 含O2水蒸汽环境的腐蚀增重。NaCl盐雾环境下GH4169合金的腐蚀产物为Fe2O3、NiFe2O4、Cr2O3和NaNbO3,腐蚀产物膜为单层结构且相对致密;而合金在固态NaCl + 含O2水蒸汽环境下的腐蚀产物较复杂,腐蚀产物膜厚而疏松。GH4169合金中的缺陷和晶界是Cl的快速传输通道,对腐蚀的发生有促进作用。
(2) NaCl盐雾环境下GH4169合金初期腐蚀机制为氧化与氯的活性氧化腐蚀机理共同作用加速腐蚀;随着NaCl沉积量的增加,GH4169合金腐蚀逐渐转变为以氯的活性氧化腐蚀机理为主的加速腐蚀。
(3) GH4169合金的氧化物在600℃下NaCl腐蚀环境中的敏感性顺序为:TiO2 > MoO2 > Cr2O3(Nb2O5) > Fe2O3 > Al2O3 > NiO。根据M-Cl-O相平衡图确定,GH4169合金内各元素在中温下对氯活化腐蚀敏感性的排序依次为:Ti > Al > Nb、Cr > Fe > Mo、Ni。
来源--金属学报





 沪公网安备31011202020290号
沪公网安备31011202020290号
