分享:DZ445镍基高温合金高温长时间氧化形成的多层膜结构
刘来娣1,2, 丁彪 ,1,2, 任维丽
,1,2, 任维丽 ,1,2, 钟云波1,2, 王晖3, 王秋良3
,1,2, 钟云波1,2, 王晖3, 王秋良3
研究了高Cr / Al比和中Ta含量的DZ445镍基高温合金在900℃下300~2600 h的氧化行为。结果表明,900℃氧化≥ 500 h,氧化膜呈现多层结构,最外层氧化物相为NiCr2O4、Cr2O3和TiO2,次外层为CrTaO4和TiO2,次内层为Al2O3、NiCr2O4和NiO,最内层主要是Al2O3。次外层和次内层的出现使得合金氧化速率降低,表现为动力学方程的指数大幅度增加和氧化速率常数急剧下降。这2层的出现也使得合金氧化机理发生转变,次外层形成后氧化过程由合金元素Cr、Ti、Ni向外扩散转变为由Al的向外扩散和O的向内扩散所控制;次内层形成后,氧化过程转变为Ni、Cr的向外扩散和O的向内扩散所控制。这种多层氧化膜结构使得DZ445合金表现出优异的抗氧化能力。
关键词:
镍基高温合金具有优异的高温力学性能和抗氧化性能,广泛应用于航空发动机和燃气轮机涡轮叶片等热端部件[1~3]。在高温恶劣的工作环境下,该材料的抗氧化能力是当前研究的热点。提高材料抗氧化能力的主要方法有在合金表面覆盖热障涂层[4,5]和添加抗氧化元素。在添加的合金元素中,Cr和Al可以氧化生成含有Al2O3和Cr2O3的结构致密的保护性氧化膜,成为镍基高温合金中的主要抗氧化元素。这2个元素含量的比值会影响氧化膜中的物相种类,当Cr / Al比较高时,氧化膜主要是Cr2O3;比值较低时,氧化膜主要是Al2O3[6]。镍基合金体系不同,氧化膜出现Cr2O3 / Al2O3对应的Cr / Al比不同。Giggins和Pettit[7]研究Ni-(5~30)Cr-(1~6)Al (质量分数,%,下同)系列合金的氧化行为时,得出Cr含量高(> 10%,质量分数,下同)而Al含量低(< 2%)即Cr / Al比大于5时,形成的氧化膜外层主要是Cr2O3,内层是Al2O3;当合金中Al含量高(> 4%)时,Cr / Al比小于5,其氧化膜仅为Al2O3。Barrett和Lowell[8]研究Ni-(0~37)Cr-(0~32)Al合金氧化行为时发现,Cr含量高(> 18%)且Al含量低(< 5%)时,Cr / Al比大于3.6,氧化外层主要由Cr2O3构成;当Al含量高(> 5%)时,氧化层则由Al2O3构成。Chen等[9]研究表明,72.6Ni-16.7Al-10.7Cr合金Cr / Al比为0.64,氧化层外层为Al2O3,中间层为尖晶石NiAl2O4和Cr2O3,内层为NiO。
Ta元素对镍基高温合金氧化行为也有显著影响,它的作用受合金中其他元素的影响,也与其加入量有关。Yang[10]对Ni-12.8Al-4.8Cr-4.2Co-1.6W-3.1Mo-1.0Re合金进行高温氧化对比实验,发现加入3.0%Ta后氧化层由外层NiO和内层Al2O3组成,Ta促进了保护性Al2O3氧化层的形成,提高了合金抗氧化性;而加入8.8%Ta导致合金无法形成稳定的Al2O3,形成的NiTa2O6等复杂氧化物反而使合金抗氧化性降低。Kim等[11]在研究Ni-(10~16)Cr-5Al-(3~6)Ta合金的氧化行为时发现,在1000℃高温下,Ta的氧化物能够显著提高合金的抗氧化性。Park等[12]对Ni-(8~15)Cr-(3~8)Al-(0~10)Ta合金在1000℃下氧化300 h研究发现,在Al含量低的时候,Ta含量的变化比Cr元素对氧化行为的影响更显著;而高Al含量下,Ta和Cr含量的变化对氧化行为影响不明显。Han等[13]研究Ni-12Cr-4.2Al-(3.8~5.8)Ta合金时发现,含5.8%Ta合金的氧化速率低于含3.8%Ta的合金,这是因为在高Ta含量的高温合金中形成了连续致密的CrTaO4。Park等[14]研究Ni-8Cr-(4~5)Al-(3~6)Ta合金的结果显示,添加5%Ta会减慢Al2O3的形成,使镍基高温合金在850℃条件下抗氧化性下降;当Ta含量大于5%,Ta可以降低O活性或限制Al在氧化层中的向外扩散,增强合金的抗氧化性。Liu等[15]和Guo等[16]研究认为,Ta会降低Al的向外扩散速率,从而抑制DD32M合金和β-NiAl合金表面氧化层的生长。可以看出,Ta对镍基高温合金的抗氧化性能的影响是通过影响Al、Cr等合金元素的氧化物种类而发生作用的,当Ta含量达到3%时就可以提高合金抗氧化性能,高Ta含量(如8.8%)对合金抗氧化性能产生有害影响,而中等Ta含量(5%~6%)对抗氧化性能的影响因合金种类差异而不同。
DZ445合金含有14%Cr、4%Al和5%Ta,前期研究[17]表明,其外层氧化物主要是Cr2O3,属于高Cr / Al比和中Ta含量的镍基合金体系;分析了该合金在850~900℃下300 h的氧化行为,发现CrTaO4的形成使合金的氧化速率降低,氧化速率常数从3.10 × 10-3 mg2/(cm4·h)变为4.71 × 10-4 mg3/(cm6·h),激活能从335 kJ/mol变为423 kJ/mol。考虑到合金长时间服役,本工作进一步考察了DZ445在900℃下长达2600 h的氧化行为,分析该合金长时间氧化产物、氧化膜结构和氧化动力学及其氧化机制。发现长时间氧化条件下该合金氧化膜形成多层结构,这种多层结构使得该合金呈现出优异的抗氧化能力。
1 实验方法
实验采用DZ445高温合金,化学成分如表1所示。该合金的制备工艺如下:真空感应熔炼炉熔炼并浇注成母合金锭,以7 mm/min抽拉速率在定向凝固炉中拉制成直径16 mm、长200 mm的合金圆棒。随后进行热处理,工艺为:1210℃、2 h、AC + 1080℃、2 h、AC + 850℃、24 h、AC (AC为空冷)。
表1 DZ445镍基高温合金的化学成分
Table 1
| Composition | Co | Cr | Mo | W | Al | Ti | Ta | C | Zr | Ni |
|---|---|---|---|---|---|---|---|---|---|---|
| Mass fraction / % | 10.00 | 14.00 | 1.50 | 4.00 | 4.00 | 3.00 | 5.00 | 0.08 | 0.03 | Bal. |
| Atomic fraction / % | 9.90 | 15.70 | 0.90 | 1.30 | 8.70 | 3.70 | 1.60 | 0.39 | 0.02 | Bal. |
在热处理后的试棒上通过线切割制成尺寸为10 mm × 10 mm × 3 mm的样品用作氧化实验。试样表面经SiC砂纸水磨至2000号,之后用6 μm金刚石抛光膏进行抛光。用千分尺测量抛光后的样品尺寸,并计算其表面积。随后,将研磨好的试样放入酒精中用高频超声波清洗以保证表面清洗干净。氧化实验前,用清水、酒精清洗Al2O3坩埚,去除其表面油污,并在900℃下保温24 h,以去除杂质,确保氧化过程中质量稳定。将试样放入坩埚一起称重,作为其初始重量,最后将样品放入马弗炉中分别在850、900和925℃进行300~2600 h等温氧化实验。
采用不连续称重法测定样品的氧化增重以确定其动力学曲线。在选定的时间点(3 h、6 h、12 h、24 h、48 h、72 h、96 h、120 h、…、2600 h),从炉中将坩埚和样品一起取出空冷至室温,使用精度为10-4 g电子天平称重。同时,对氧化不同时间后的样品利用D/MAX2000V PC X射线衍射仪(XRD)、VEGA 3 Easy Probe扫描电子显微镜(SEM)及其附带的能谱仪(EDS)研究氧化物的相组成、表面形貌、横截面形貌和氧化层的元素组成。
观察样品横截面时,需要先对样品进行化学镀镍,再进行金相制备。首先在室温下把样品放入13 g/L SnCl2·2H2O + 40 mL HCl +去离子水溶液中敏化处理2 min,然后放入0.2 g/L PdCl2 + 7 mL HCl + 去离子水溶液中活化处理0.5~1 min,最后在85~90℃的水浴锅中进行化学镀镍,化学镀液为23~28 g/L NiSO4·6H2O + 25~35 g/L NaH2PO2·H2O + 10~16 g/L Na3C6H5O7·2H2O + 10~15 g/L CH3COONa + 10~16 g/L C3H6O3 +去离子水,时间约为60 min,溶液的pH值为4~5。组织观察用腐蚀剂为5 g CuSO4 + 10 mL HCl + 20 mL H2O,腐蚀时间为45 s。
2 实验结果
2.1 氧化物相分析
DZ445合金在900℃氧化不同时间后的XRD谱如图1所示。可以看出,不同时间的氧化产物种类基本一致,主要包括NiCr2O4、TiO2、Cr2O3、CrTaO4和Al2O3。与氧化300 h相比,氧化500 h的XRD谱中Cr2O3的衍射峰数量减少,NiCr2O4的衍射峰数量增加,TiO2衍射峰强度提高,表明氧化表层中Cr2O3的含量减少,NiCr2O4和TiO2含量增加。氧化500 h后,表面氧化物的种类随时间延长保持稳定。但氧化不同时间的XRD谱中,都没有W、Co和Mo的氧化物。
图1

图1 DZ445镍基高温合金在900℃氧化不同时间的XRD谱
Fig.1 XRD spectra of the DZ445 Ni-based superalloy after the oxidation at 900oC for different time
2.2 表面形貌
图2是DZ445合金在900℃氧化不同时间表面形貌的SEM像。可见,氧化时间≤ 915 h,氧化膜致密完整,基本没有剥落产生;氧化时间≥ 1100 h,氧化膜出现剥落,随时间的延长剥落程度加剧,但是剥落程度并不严重,在氧化2600 h时剥落面积约10%。这可能是合金在空冷过程中遭遇剧烈的温度变化使得氧化层内应力分布不均匀,或者氧化膜与基体的膨胀系数存在差异导致的[14,18,19]。
图2

图2 900℃下DZ445镍基高温合金氧化不同时间表面形貌的SEM像
Fig.2 SEM images of the surface of the DZ445 Ni-based superalloy oxidized at 900oC for 500 h (a), 915 h (b), 1100 h (c), 1500 h (d), 1800 h (e), 2200 h (f), and 2600 h (g) (A and B in Fig.2a indicate bright white part and dark black part of oxide film, respectively)
其次,氧化膜表面无脱落的区域由大部分亮白色和少部分暗黑色的区域构成,分别标记为A和B区域(在氧化时间为500 h时,分别约占总面积的95%和5%)。随氧化时间延长,A区域面积增大,B区域面积逐渐减小。EDS分析结果(表2)表明,A区域中Al元素含量远低于B区域,分别为2.04%和25.25% (原子分数)。推测这是合金原始组织中枝晶干与枝晶间的Al含量不同导致的,由于枝晶干先凝固,Al元素又是正偏析元素,不断地被排出到枝晶间区域[20]。所以亮白色和暗黑色区域应该分别对应着合金原始的枝晶干和枝晶间区域。
表2 DZ445镍基高温合金在900℃氧化500 h后表面氧化膜不同区域的元素分布 (atomic fraction / %)
Table 2
| Area | O | Al | Cr | Ni | Ti | Ta | Co |
|---|---|---|---|---|---|---|---|
| A | 61.83 | 2.04 | 17.00 | 11.32 | 5.94 | 0.08 | 1.79 |
| B | 60.28 | 25.25 | 4.40 | 7.96 | 1.08 | 0.03 | 1.00 |
2.3 横截面形貌
图3是ZD445合金在900℃氧化不同时间后横截面形貌的SEM像。可以看出,氧化不同时间后的氧化膜都呈现出多层结构。氧化300 h时,氧化膜为最外层、次外层和最内层的3层结构,分别标记为P1、P2和P4 (图3a)。从氧化500 h开始(图3b~h),氧化膜演变为4层结构,从外到内依次定义为最外层、次外层、次内层、最内层,分别用P1、P2、P3和P4来标记,各个层内的EDS分析结果如表3所示。可见,最外层P1主要富含Cr、Ni和O,结合XRD结果推测该层物相主要是Cr2O3和尖晶石NiCr2O4;次外层P2主要含有Ta、Ti和O元素,推测其主要氧化物是CrTaO4和TiO2;最内层P4主要含Al和O元素,主要氧化物是Al2O3;次内层P3与最内层P4相比,其Al含量降低,Ni 和Cr含量增加,推测该层中主要氧化物有Al2O3、NiO和NiCr2O4。
图3

图3 DZ445镍基高温合金在900℃氧化不同时间横截面形貌的SEM像
Fig.3 SEM images of the cross-section of the DZ445 Ni-based superalloy oxidized at 900oC for 300 h (a), 500 h (b), 915 h (c), 1100 h (d), 1500 h (e), 1800 h (f), 2200 h (g), and 2600 h (h) (P1, P2, P3, and P4 indicate the outermost layer, subouter layer, subinner layer, and innermost layer, respectively. The bright edge on the top of the outermost layer is nickel plated)
表3 DZ445镍基高温合金在900℃氧化不同时间后的氧化膜各层元素分布的EDS分析 (atomic fraction / %)
Table 3
| Oxide layer | Time / h | Al | Cr | Ta | Ti | Ni | O | Co |
|---|---|---|---|---|---|---|---|---|
| P1 | 300 | 1.11 | 32.03 | 0.00 | 2.05 | 1.77 | 62.64 | 0.40 |
| 500 | 3.32 | 19.35 | 0.18 | 3.59 | 10.65 | 58.36 | 4.56 | |
| 915 | 0.69 | 28.19 | 0.06 | 1.60 | 5.38 | 62.54 | 1.54 | |
| 1100 | 3.30 | 21.54 | 0.17 | 2.31 | 10.64 | 57.94 | 4.09 | |
| 1500 | 1.76 | 16.81 | 0.12 | 7.12 | 14.59 | 55.35 | 4.24 | |
| 1800 | 5.43 | 16.38 | 0.18 | 4.59 | 8.49 | 61.37 | 3.57 | |
| 2200 | 2.69 | 20.75 | 0.07 | 1.52 | 11.36 | 58.75 | 4.87 | |
| 2600 | 2.20 | 21.02 | 0.22 | 1.80 | 10.29 | 62.13 | 2.34 | |
| P2 | 300 | 4.58 | 11.30 | 6.14 | 8.11 | 1.13 | 68.61 | 0.15 |
| 500 | 2.63 | 10.42 | 6.49 | 7.64 | 5.98 | 65.13 | 1.72 | |
| 915 | 1.09 | 6.72 | 9.37 | 8.36 | 4.51 | 69.75 | 0.23 | |
| 1100 | 4.22 | 6.69 | 7.29 | 6.79 | 3.45 | 71.07 | 0.50 | |
| 1500 | 1.36 | 10.97 | 6.95 | 8.65 | 7.00 | 63.13 | 1.96 | |
| 1800 | 2.12 | 9.64 | 7.54 | 8.21 | 3.28 | 68.16 | 1.05 | |
| 2200 | 1.53 | 8.89 | 7.14 | 8.03 | 4.85 | 68.33 | 1.23 | |
| 2600 | 0.73 | 6.53 | 9.26 | 8.58 | 3.75 | 70.90 | 0.25 | |
| P3 | 300 | - | - | - | - | - | - | - |
| 500 | 24.43 | 3.55 | 0.82 | 1.21 | 11.94 | 56.75 | 1.32 | |
| 915 | 14.27 | 3.04 | 1.14 | 1.03 | 15.43 | 64.82 | 0.28 | |
| 1100 | 27.66 | 1.46 | 0.38 | 0.44 | 9.71 | 59.57 | 0.77 | |
| 1500 | 23.14 | 3.90 | 0.21 | 0.28 | 17.83 | 53.29 | 1.34 | |
| 1800 | 22.94 | 4.47 | 0.83 | 1.27 | 10.50 | 58.72 | 1.27 | |
| 2200 | 21.70 | 4.67 | 0.20 | 0.62 | 15.97 | 55.44 | 1.40 | |
| 2600 | 20.97 | 3.02 | 0.49 | 0.42 | 12.67 | 61.35 | 1.07 | |
| P4 | 300 | 36.55 | 0.77 | 0.18 | 0.24 | 2.62 | 59.12 | 0.51 |
| 500 | 33.37 | 2.30 | 0.32 | 0.41 | 3.14 | 59.47 | 0.99 | |
| 915 | 34.07 | 1.97 | 0.19 | 0.30 | 4.56 | 58.05 | 0.88 | |
| 1100 | 35.85 | 1.18 | 0.15 | 1.54 | 0.79 | 60.35 | 0.13 | |
| 1500 | 35.53 | 1.52 | 0.06 | 0.29 | 3.90 | 57.92 | 0.78 | |
| 1800 | 35.24 | 1.90 | 0.07 | 0.90 | 1.53 | 60.12 | 0.24 | |
| 2200 | 33.48 | 1.30 | 0.11 | 0.57 | 4.41 | 59.45 | 0.69 | |
| 2600 | 33.84 | 1.97 | 0.17 | 0.74 | 1.74 | 61.34 | 0.20 |
DZ445合金在900℃氧化不同时间后各氧化层的厚度变化曲线如图4所示。在氧化500 h后,最外层和次外层的厚度增幅很小;次内层在氧化500 h后形成,随时间增大呈现增厚的趋势;最内层厚度在整个氧化时间段表现为减小的趋势,可能原因是贫γ′层Al消耗不足,不足以维持内氧化。
图4

图4 DZ445镍基高温合金在900℃氧化不同时间后各氧化层的厚度变化曲线
Fig.4 Thicknesses of the oxidizing layer of the DZ445 Ni-based superalloy after oxidizing at 900oC for different time in air
2.4 氧化动力学
图5是DZ445合金在850、900和925℃下的氧化增重动力学曲线。其中900℃下氧化时间为2600 h,850和925℃下增重进入稳定变化时停止实验,氧化时间分别为950和910 h。可以看出,这3个温度下的氧化规律相似,初始阶段氧化增重较快,随着时间的延长其增加速率降低;在相同的时间下,温度越高,氧化增重也越大。
图5
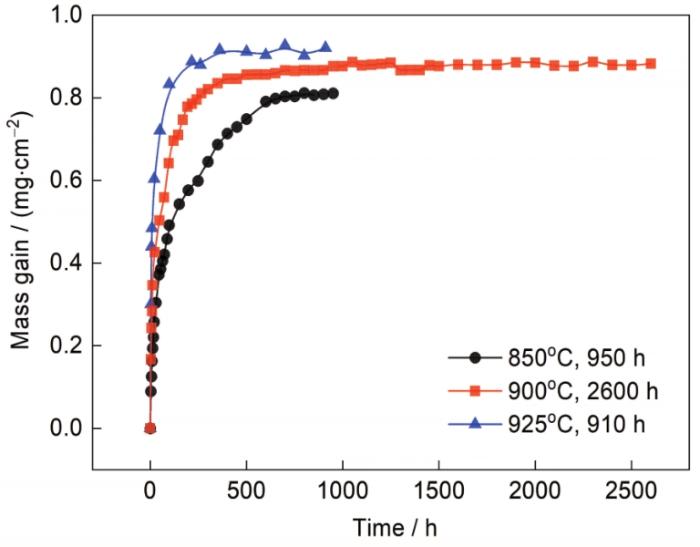
图5 DZ445镍基高温合金在不同温度下的恒温氧化动力学曲线
Fig.5 Isothermal oxidation kinetics curves of DZ445 Ni-based superalloy oxidized at 850oC for 950 h, 900oC for 2600 h, and 925oC for 910 h
式中,Δm为单位面积的氧化增重;t为氧化时间;K为恒温氧化速率常数;n是氧化动力学方程指数,反映增重对氧化时间变化的依赖程度。根据
图6

图6 DZ445镍基高温合金在不同温度下氧化增重的双对数曲线
Fig.6 Double logarithmic graphs of the mass gain (ΔW) and oxidation time (t) at different temperatures
图7

图7 lnK和1 / T的关系图
Fig.7 Logarithm of lnK plotted against the temperature reciprocal (1 / T) before and after the formation of the continuous subouter layer and subinner layer
表4 900℃下不同时段的氧化动力学方程指数(n)、恒温氧化速率常数(K)和氧化激活能(E)
Table 4
| Time | n | K | E / (kJ·mol-1) |
|---|---|---|---|
| Before the formation of CrTaO4 layer | 2.17 | 1.0 × 10-2 mg2·cm-4·h-1 | 325 |
| Between the formation of subouter and subinner layer | 4.17 | 1.93 × 10-3 mg3·cm-6·h-1 | 424 |
| After the formation of subinner layer | 25.00 | 3.5 × 10-5 mg25·cm-50·h-1 | 485 |
由图6可知,850、900和925℃下的氧化双对数拟合直线均存在2个拐点,结合图3和以前的工作[17],这2个拐点分别对应着连续完整的CrTaO4次外层和次内层的出现,比如,900℃下2个拐点分别在24和500 h处,而这2个时间分别对应着氧化膜中连续完整的CrTaO4次外层和次内层的形成(图3),850℃时2个拐点分别在96和600 h处,925℃时分别在12和98 h处。由表4可知,CrTaO4层形成前n值为2.17,在CrTaO4层形成后到次内层形成前n值为4.17,次内层形成后n值为25.00。
K与温度的关系可以通过Arrhenius公式来表达[20,21]:
式中,E为氧化激活能,A为指前因子,R为气体常数,T为绝对温度。通过lnK-1 / T关系曲线的斜率(图7),可以获得E。计算得出在所研究的温度范围段,不同n值对应的3个不同氧化阶段的激活能分别为325、424和485 kJ/mol。
3 分析讨论
由以上结果可知,在所研究的温度范围段,DZ445合金长时间氧化后其膜层形成4层结构:最外层氧化物相主要是Cr2O3、NiCr2O4和TiO2,次外层主要物相为CrTaO4和TiO2,次内层为Al2O3、NiCr2O4和NiO,最内层为Al2O3。次外层和次内层的形成改变了氧化速率方程指数,降低了氧化速率常数。
3.1 最外层、次外层和最内层的物相构成
DZ445合金在氧化不同阶段氧化膜各层中主要物相种类不一样,这主要是由合金中元素含量、与O发生反应的自由能及其扩散能力决定的。反应自由能越低,越容易发生反应;某一元素含量越高,扩散能力越大,该元素氧化物越容易形成。
首先从热力学自由能角度来分析,DZ445合金基体元素是Ni,并主要含有Cr、Co、Al、Ti、Ta、Mo和W等元素,这些元素均能与O反应生成氧化物。900℃下这些氧化物生成的Gibbs自由能(ΔG)大小依次为:ΔG
表5 900℃下DZ445镍基高温合金元素氧化物生成的Gibbs自由能(ΔG)[17,21,23] (kJ·mol-1)
Table 5
| Oxide | ΔG | Oxide | ΔG |
|---|---|---|---|
| NiO | -279.2 | NiCr2O4 | -826.2 |
| Cr2O3 | -547.1 | CrTaO4 | -580.3 |
| TiO2 | -733.4 | CoO | -274.9 |
| Al2O3 | -869.2 | WO2 | -379.7 |
| Ta2O5 | -613.5 | MoO2 | -382.9 |
由于Co的氧化反应Gibbs自由能变化大于基体Ni,WO2和MoO2在高温下易挥发[17,27~30],因此氧化膜检测不到CoO、MoO2和WO2的存在。氧化物中也没有观察到AlTaO4,可能是由于DZ445合金的Cr含量远高于Al,当Al 含量高且Cr含量低时合金氧化才能形成AlTaO4,如TMS-82+合金[26]含12.24%Al和5.42%Cr,因此其氧化物中可以检测到AlTaO4。
DZ445合金中Cr的含量比Al高,Cr在合金中沿晶界短程扩散的速率明显高于Al元素[31,32],所以氧化初期以Cr的选择性氧化为主,快速形成大量Cr2O3覆盖在合金表面。同时,尽管基体中的Ti含量低,但900℃下Ti扩散比Cr、Al快[22,33],其扩散系数分别为6.00 × 10-16 [34]、2.46 × 10-16 [17]和7.62 × 10-18 [35] m2/s,所以氧化初始时会生成少量TiO2,其他合金如GH4037[36]、GTD-111[37]、Fe-33Ni-19Cr[38]在氧化初期的外氧化层也会出现TiO2或含Ti氧化物。此外,由于Ni是DZ445合金的基体元素,其含量超过50%,远远大于其他元素,易与O反应产生NiO。随着氧化的进行,NiO会与Cr2O3固相反应生成尖晶石NiCr2O4,因此逐渐形成由NiCr2O4、Cr2O3和TiO2组成的外氧化层。
Ta向外扩散与O反应倾向于形成Ta2O5[17,31,39],随着氧化的进行,Ta2O5会与Cr2O3反应生成CrTaO4。Ta在镍基合金中的扩散速率比Cr慢40% (Ta扩散系数为1.45 × 10-16 m2/s[40]),比Al快2个数量级,所以CrTaO4形成的位置在Cr2O3层之下、Al2O3层上方[33,37,41],因此在氧化一段时间后紧次于最外层形成连续的CrTaO4层。对应本工作中900℃氧化24 h出现3层氧化膜结构。925和850℃分别对应12和96 h,因此温度越高,出现连续CrTaO4层的时间越短。
Al在Al2O3中的自扩散系数(1.68 × 10-22 cm2/s[42])比Cr和Ti在其氧化物中的自扩散系数(5.98 × 10-14 [42]和2.00 × 10-14 [43] cm2/s)小8个数量级,在合金中的扩散系数也比Cr、Ti、Ta小2个数量级,扩散速率很慢,Al更倾向于与扩散进来的O发生反应生成Al2O3[22]。所以虽然Al与O的反应自由能很低,但是由于其低的含量和低的扩散能力,形成于氧化膜层的最内层。
3.2 次内层的形成及其物相构成
次内层氧化物相种类主要是Al2O3、NiCr2O4和NiO,位于次外层(CrTaO4层)和最内层(Al2O3)之间,它的形成是由其邻接的最内层与次外层对元素的屏障作用和合金元素通过贫γ′层的扩散能力决定的。
首先,最外层和次外层的成分基本上随时间的增长不再发生变化(图3和表3),说明这2层对合金元素的向外扩散起到了很好的屏障作用,尤其是次外层的连续CrTaO4层,之前的研究[13,17,44,45]表明该层的出现能够显著降低氧化速率。这可以通过对比CrTaO4、NiCr2O4、Cr2O3和Al2O3的晶体结构的原子排列致密度来进一步佐证,如图8所示。虽然这几种氧化物晶体结构不同,CrTaO4是金红石结构[46],NiCr2O4是尖晶石结构,Cr2O3与Al2O3 (α-Al2O3)都是刚玉型结构[47],但是其中的O2-都近似密排六方紧密堆积,阳离子填充在八面体间隙或四面体间隙中。CrTaO4结构中的阳离子填充在八面体间隙(图8a),NiCr2O4结构中Cr3+占据晶格中的八面体间隙,Ni2+位于四面体间隙(图8b),Cr2O3和Al2O3 (α-Al2O3)结构中的Cr3+和 Al3+同样占据晶格中的八面体间隙(图8c和d)。Ta5+、Cr3+、Al3+、Ni2+和O2-的离子半径分别为0.064、0.062、0.054、0.069和0.132 nm,Cr2O3、Al2O3、NiCr2O4和CrTaO4的致密度分别为21.33%、20.87%、58.59%和(62.17~62.55)%,CrTaO4的致密度最大,NiCr2O4次之。高的致密度使得其构成原子和其他原子扩散通过它的阻力增大[48],扩散系数减小,扩散激活能增大。因此,CrTaO4层更能有效地抑制Cr、Ti及其他合金元素的向外扩散和O原子的向内扩散,NiCr2O4对原子扩散的屏蔽作用次之,Cr2O3和Al2O3阻止元素扩散作用再次之。
图8

图8 CrTaO4、NiCr2O4、Cr2O3和Al2O3的晶体结构
Fig.8 Crystal structures of oxides CrTaO4 (a), NiCr2O4 (b), Cr2O3 (c), and Al2O3 (d)
其次,次内层的形成也由内部基体中合金元素的扩散驱动力决定,而扩散驱动力与浓度梯度有关。Wagner理论[49]和文献[50]均指出,金属/氧化物界面的氧化反应驱动力为金属与O形成氧化物的自由能变化和氧化膜中成分的浓度梯度。图9是Al、Ni、Cr元素在氧化300和500 h时从最内层(或次内层)到基体的浓度梯度曲线。可见,氧化300和500 h的浓度梯度变化趋势基本一致。在氧化层/基体界面,Ni的浓度梯度最大,Cr次之,Al的浓度梯度为负,这说明此时Ni、Cr从基体向氧化层扩散的扩散驱动力比Al更大,能不断从基体向氧化层扩散。与氧化300 h相比,氧化500 h以后Ni、Cr的浓度梯度减小,表明基体扩散过来的元素含量也在逐步降低。
图9

图9 Al、Ni、Cr元素在氧化300和500 h时从最内层(或次内层)到基体的浓度梯度曲线
Fig.9 Concentration gradient distribution curves of alloy elements Al, Ni, and Cr from the innermost layer (or subinner layer) to the matrix after oxidation for 300 h (a) and 500 h (b)
综上,次内层的形成主要取决于CrTaO4层的屏障作用以及元素的扩散驱动力。从实验结果看,氧化300 h时Ni、Cr的浓度梯度较大,说明此时Ni、Cr在CrTaO4层下分布的含量较低,不足以形成NiCr2O4和NiO,所以氧化膜只有3层结构。随着Ni、Cr逐渐从基体向外扩散,氧化500 h后形成4层氧化膜结构。
3.3 长时间氧化下各层的形成机理及其对氧化速率的影响
从上面分析讨论可以看出,DZ445合金在本工作所研究温度的范围内,氧化膜层形成了多层结构(图3),这是由各个合金元素与O结合的自由能及其浓度以及扩散能力决定的,也正是其成分特点使得氧化动力学随时间的延长发生了变化。
结合之前的工作[17],连续的CrTaO4层形成之前,氧化以Cr、Ni和Ti的扩散过程为主(图10a), 此阶段的n较小(约为2),K较大(1.0 × 10-2 mg2/(cm4·h)),E也较小(325 kJ/mol),表明此时氧化速率较快;CrTaO4层形成之后,氧化过程以O向内的扩散和Al原子向外扩散为主(图10b),此时n增大,K减小一个数量级(1.93 × 10-3 mg3/(cm6·h)),E增大为424 kJ/mol,这源于Al原子在基体和氧化膜中的扩散激活能大于Cr、Ni和Ti[17,43,51~53];随着氧化时间的进一步延长,此时氧化膜和基体贫γ′界面附近Ni、Cr浓度梯度远大于Al原子,于是Ni、Cr原子向Al2O3内层扩散(图10c),Al原子向外扩散的趋势较小,形成富NiCr2O4、NiO和Al2O3的次内层,其颜色较最内层(Al2O3为主)浅(图3),此阶段对应的氧化速率进一步剧烈降低,n增大到25.00,K降低了2个数量级(3.5 × 10-5 mg25/(cm50·h)),E也进一步增大到485kJ/mol,且次内层厚度随氧化时间增加的增大幅度很小,说明次外层和次内层的形成为DZ445合金提供了优异的抗氧化能力。
图10

图10 氧化机理示意图
Fig.10 Schematics of oxidation process
(a) before the formation of CrTaO4 layer
(b) between the formation of CrTaO4 layer and subinner layer
(c) after the formation of subinner layer
4 结论
(1) 高Cr / Al比和中Ta含量的DZ445镍基高温合金在900℃下恒温氧化300 h后,氧化膜由外氧化层、次外层和内层构成;在氧化时间≥ 500 h时,在次外层和最内层之间增加了次内层。最外层氧化物相为NiCr2O4、Cr2O3和TiO2,次外层为CrTaO4和TiO2,次内层为Al2O3、NiCr2O4和NiO,最内层主要是Al2O3。
(2) DZ445合金在氧化初期动力学方程指数为2.17,符合平方规律。随着氧化时间的延长,次外层和次内层逐渐形成,动力学方程指数分别增大到4.17和25.00,激活能也分别增大到424和485 kJ/mol。表明这2层的出现使得氧化速率大幅降低,显著增强了合金的抗氧化能力。
(3) 在初期CrTaO4次外层没形成之前,DZ445合金的氧化过程由合金元素向外扩散控制;在CrTaO4层形成之后由Al的向外扩散和O的向内扩散所控制;次内层形成后,氧化过程转变为Ni、Cr的向外扩散和O的向内扩散所控制。
来源--金属学报





 沪公网安备31011202020290号
沪公网安备31011202020290号
